Один из ведущих в мире специалистов по изучению структуры генома Сергей Разин рассказал корреспонденту «Научной России» о способах упаковки хромосом в клетках различных организмов и о том, как это связано с теми или иными заболеваниями. Мы поговорили о том, что такое топологически ассоциированные домены (ТАД), которые сегодня находятся на острие научных открытий, и почему рак тесно связан с пространственной организацией генома, а также обсудили роль некодирующих ДНК в развитии этого заболевания. Подробнее ― в нашем интервью.
Справка: Сергей Владимирович Разин ― доктор биологических наук, член-корреспондент РАН, профессор, главный научный сотрудник, руководитель отдела клеточной геномики и заведующий лабораторией структурно-функциональной организации хромосом Института биологии гена РАН, заведующий кафедрой молекулярной биологии биологического факультета МГУ им. М.В. Ломоносова.
― Вы специалист в достаточно новой области знания ― 3D-геномике. Как в ней рассматривают геном?
― Еще десять лет назад термин «3D-геномика» вызывал непонимание даже у биологов, поскольку ДНК ― это линейный полимер и, казалось бы, какое отношение к ней имеет трехмерная пространственная организация? Чтобы понять, чем мы занимаемся, нужно сначала вспомнить, что представляет собой эукариотический геном и как он эволюционировал.
Гены, кодирующие белки, очень схожи у разных животных и у человека. Можно сказать, что они практически идентичны у людей и, например, у обезьян, мышей и даже рыб. Все потому, что наша эволюция шла путем резкого усложнения систем, регулирующих гены, а не самих генов.
Гены человека, как и остальных эукариот, то есть организмов, чьи клетки содержат ядро, регулируются промоторами ― специальной последовательностью нуклеотидов, располагающихся в начале гена, и так называемыми энхансерами, которые, в свою очередь, могут находиться где угодно, в том числе далеко от промотора. В процессе нашей эволюции, особенно на этапе перехода от приматов к человеку, количество энхансеров резко возросло, и сегодня мы знаем, что на один ген их может приходиться более десяти. В разных ситуациях в организме могут использоваться разные комбинации энхансеров — например, для того, чтобы клетки могли лучше адаптироваться к каким-то внешним условиям или отвечать на какие-то сигналы. Энхансеры представляют собой площадки, с которыми связываются различные регуляторные белки, в том числе транскрипционные факторы и различные компоненты транскрипционной машины. Затем все это определенным способом передается на промотор. Но как это можно сделать? Самый простой способ состоит в том, чтобы разместить энхансер рядом с промотором в физическом пространстве клеточного ядра.
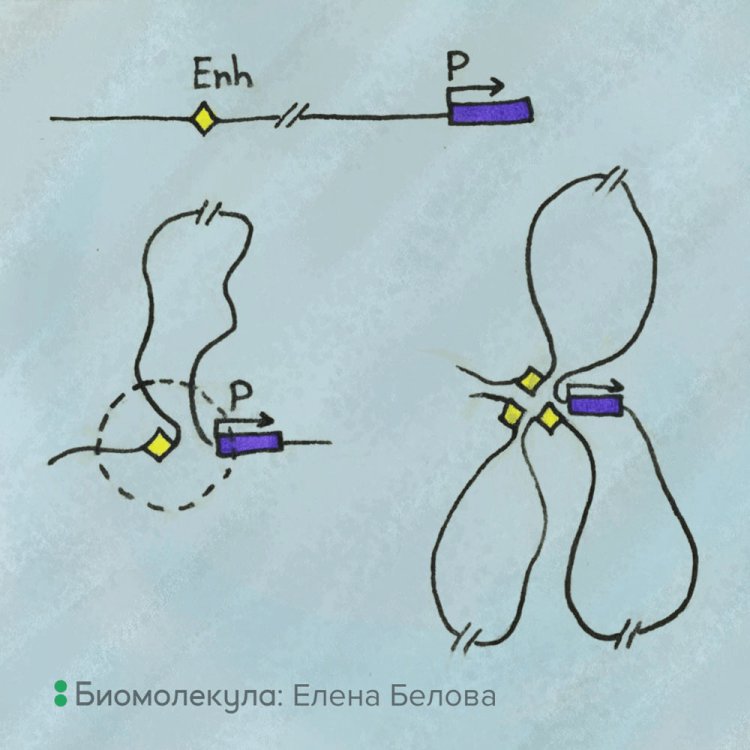
Энхансеры и промоторы часто находятся далеко друг от друга на молекуле ДНК. И для того чтобы они оказались рядом, должно произойти выпетливание разделяющего их фрагмента ДНК, то есть образование самой настоящей петли из ДНК, в основании которой будут находиться энхансер и промотор.
Такая система позволяет собирать разные комбинации энхансеров, поскольку вы можете сделать сколько угодно разных петель, приблизив таким образом к промотору несколько энхансеров. Кроме того, это дает возможность активировать одним блоком энхансеров сразу несколько генов, что требуется в случаях, когда эти гены участвуют в синтезе какого-то одного продукта, необходимого для реализации определенного метаболического пути.
Энхансеры (выделено желтым), стоящие далеко от своего промотора (выделено фиолетовым) в последовательности ДНК, могут быть сближены в пространстве с помощью выпетливания хроматиновой фибриллы, представляющей собой один из уровней упаковки хроматина ― вещества, из которого состоят хромосомы. Иллюстрация: Елена Белова / Биомолекула
― Как описываемая вами пространственная организация генома может быть связана с различными заболеваниями?
― Важно понимать, что в микромире, о котором мы говорим, все постоянно движется, различные элементы, в том числе куски хромосом, перемещаются относительно друг друга. Если мы имеем дело с очень сложным и большим геномом, таким как человеческий, то иногда рядом с энхансером может оказаться не тот промотор — например, промотор онкогена, который не должен работать в этих клетках. Так, система, исходно дающая большие преимущества, в то же время может стать причиной серьезных недостатков, в том числе нарушения регуляции работы генов. Эволюция придумала решение для этой проблемы еще на стадии появления многоклеточных организмов, разбив геном на отдельные структурно-функциональные блоки. Мы называем их топологически ассоциированными доменами (ТАД). Все описанные выше манипуляции, перемещения частей хромосомы в пространстве клеточного ядра, образование петель и т.д., как правило, происходят внутри каждого такого блока, а не за его пределами, то есть пространственные контакты ограничиваются границами ТАД.
― А как выглядят эти ТАД?
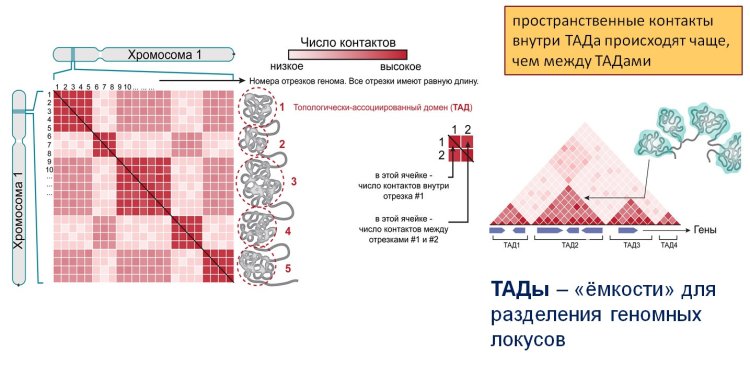
― Эти структурно-функциональные блоки представляют собой клубки, сферические или полусферические структуры, организованные из хроматиновой фибриллы внутри хромосомы. У разных клеток ТАД могут немного различаться по форме. И если раньше все это выводилось чисто биоинформатическим методом, из карт пространственной организации генома (где ТАД выглядят как треугольники), то сегодня у ученых появилась возможность визуализировать именно клубки, окрасив их с помощью специфических красителей, связывающихся только с определенными фрагментами ДНК. ТАД ограничивают сферу действия энхансеров, которые в основном активируют те гены, которые находятся внутри ТАД. Исчезновение границы, разделяющей ТАД, может приводить к нарушению регуляции и другим неприятным последствиям.
— Как давно на геном стали смотреть подобным образом?
— Любая экспериментальная наука зависит от появления новых методов: например, когда был изобретен микроскоп, мы впервые увидели микромир, о существовании которого раньше не подозревали. Что касается 3D-геномики, то в 2002 г. появился метод под названием Chromosome Conformation Capture, позволивший идентифицировать фрагменты ДНК, находящиеся рядом друг с другом в физическом пространстве клеточного ядра. На основании этого впервые были построены карты пространственной организации генома, то есть от простых рассуждений на эту тему мы смогли перейти к анализу конкретных данных. В течение многих лет любимой моделью биологов был домен бета-глобиновых генов, потому что он хорошо изучен; кроме того, глобиновые гены часто нарушаются при различных заболеваниях. Именно на примере этого домена впервые было продемонстрировано, что энхансеры действительно собираются в блоки, к которым привлекаются работающие в данный момент гены. Позже с использованием методов, основанных на фиксации конформации хромосомы, были обнаружены ТАД.
— То есть эти ТАД, эти клубки — не просто красивое визуальное представление нашего генома, а его полноценные функциональные блоки?
— Более того, не просто функциональные, а структурно-функциональные. Очень важно, что в данном случае структура оказывается связанной с функцией. Представьте себе какое-нибудь государство, в котором есть свои области, районы и т.д. Управление таким государством всегда идет по некой иерархии, но на каждом его уровне есть свои изолированные системы, обладающие определенной степенью автономии. Так и здесь: ТАД — это функциональные единицы генома, обладающие определенной степенью автономии. Исследовать их очень интересно.
— Такой взгляд на пространственную организацию генома уже отражен в учебниках, например вузовских, или мы все еще склонны рассматривать геном в линейных представлениях?
— В июне этого года вместе с моим коллегой Сергеем Владимировичем Ульяновым мы издали новый учебник для студентов-биологов под названием «Хроматин и эпигенетика», где обсуждаемые выше вопросы представлены достаточно подробно. Он был создан на основе курса лекций, который я читаю на кафедре молекулярной биологии биологического факультета МГУ им. М.В. Ломоносова. Это действительно очень хороший учебник, которого еще не было в России, да и за рубежом подобных книг не так много. Я думаю, что он будет востребован и принесет пользу будущим ученым.
Карта пространственной организации генома. Топологически ассоциированные домены (ТАД). Источник: презентация С.В. Разина / ИБГ РАН
— Давайте вернемся к вопросу связи различных заболеваний с ТАД. Могут ли эти клубки свернуться неправильно или повредиться, что приведет к негативным последствиям для здоровья?
— Генетически обусловленные заболевания можно разделить на две большие группы. Первая связана с физическим повреждением тех или иных генов. Такие поломки часто происходят с глобиновыми генами, кодирующими белки, которые входят в состав гемоглобина. Подобные нарушения приводят, например, к нарушению синтеза гемоглобина ― заболеванию под названием «таллассемия». Вторая группа заболеваний ассоциирована с ситуациями, где сам ген не поврежден, но почему-то работает не так или не там, где нужно (и это встречается гораздо чаще, чем проблемы со здоровьем, вызванные именно поломкой генов). В таких случаях речь уже идет о нарушении многоуровневых регуляторных систем, которые контролируют тот или иной ген и определяют, когда ему работать, а когда нет. И здесь очень полезной оказывается 3D-геномика, позволяющая объяснить многие из этих случаев. Есть целое научное направление под названием Genome-wide association study (GWAS), связанное с исследованием ассоциаций между относительно небольшими изменениями генома и предрасположенностью к тем или иным заболеваниям. Ученые, занимавшиеся этими вопросами, отмечали, что незначительные изменения генома, лежащие, как правило, вне кодирующих последовательностей, коррелируют с возникновением рака или других тяжелых заболеваний. Было накоплено большое количество статистических данных, но никто не мог понять, почему так происходит, ведь гены не повреждены. Но теперь, когда мы неплохо изучили механизмы формирования 3D-генома, стало очевидно, что даже небольшие изменения вне кодирующих областей могут влиять на его пространственную организацию.
— Вы могли бы привести еще какие-то примеры?
— Существует врожденное заболевание под названием «полидактилия», для которого характерно появление большего, чем в норме, количества пальцев на руках или ногах. Такая аномалия организации конечностей напрямую связана с тем, что в клетках организма нарушены границы между ТАД: два клубка, грубо говоря, сливаются в один, и в результате этого энхансер, находящийся в одном домене, начинает активировать гены, располагающиеся в другом. Это открытие стало первым задокументированным случаем, когда ученые доказали, что нарушение 3D-генома приводит к возникновению подобных заболеваний. Далее выяснилось, что такая ситуация, когда регуляторные элементы одной группы генов начинают активировать другую, не ту группу генов, что нужно, очень часто выступает и причиной онкологических заболеваний.
Рак в целом можно рассматривать как нарушение работы регуляторных систем. Это происходит в нашем организме постоянно: каждый день у нас возникают раковые клетки, которые благополучно уничтожаются иммунной системой. Но если происходит какой-то сбой, то они начинают бесконтрольно делиться.
— В случае если произошла какая-то проблема именно на уровне 3D-организации генома, иммунная система сохраняет способность защищать организм от раковых клеток?
— Иммунитет реагирует не на то, как изменилась пространственная организация генома, а на внешние характеристики клетки. Если система распознавания работает корректно, то раковые клетки будут убиты, а что стало причиной превращения здоровых клеток в раковые, иммунной системе по большому счету безразлично. Как правило, раковые клетки несут на своей поверхности специальные маркеры, которые и распознает наша иммунная система, а затем уничтожает такие патологические клетки.
Но онкологическое заболевание возникает тогда, когда раковых клеток стало очень много и организм не успел их уничтожить. Причиной всегда выступает некое событие в индивидуальной клетке.
Однако исследовать одну клетку в пробирке очень трудно, и ученые обычно используют в качестве исходного материала миллионы клеток. Это значит, что те результаты, которые мы видим в биохимических экспериментах, представляют собой некую «среднюю температуру по больнице»: мы видим какую-то интегральную картину из многих клеток. Около десяти лет назад мы задались целью разработать протокол, позволяющий составить карту укладки 3D-генома в индивидуальных клетках. Не буду вдаваться в подробности, но эта цель была достигнута. Итоги эксперимента были опубликованы в Nature в 2017 г. Примечательно, что они были получены в рамках дипломной работы студента нашей кафедры молекулярной биологии Ильи Михайловича Флямера.
― И что вы увидели?
― В первую очередь, очень большую вариабельность между клетками. Границы ТАД при этом оказались довольно стабильными, но то, как хромосомы уложены внутри них, иногда очень сильно различается. Это означает, что «неправильные» регуляторные контакты в контексте 3D-генома могут периодически возникать в индивидуальных клетках и это может стать причиной заболеваний, в том числе и онкологических. Не так давно мы опубликовали обзорную статью, где было показано, что большинство подобных случаев (из тех, что были задокументированы) связаны именно с раком. Это обусловлено тем, что, как я уже говорил, рак представляет собой нарушение регуляции экспрессии генов. Образование раковых клеток ― это в целом свойство нашего организма, наших клеток: они недостаточно стабильны, и в них периодически могут возникать какие-то отклонения.
― Мы говорим о причине возникновения рака. Но сможет ли наш организм уничтожить раковые клетки после того, как заболевание начнет развиваться, и зависит ли это от 3D-генома?
― То, что происходит дальше, ― вопрос скорее уже к иммунологам.
В лаборатории структурно-функциональной организации хромосом Института биологии гена РАН. Фото: Ольга Мерзлякова / «Научная Россия»
― В начале нашего разговора вы сказали, что большинство событий, приводящих к онкологическим заболеваниям, возникают в некодирующем геноме, который у человека составляет около 98%. Почему за миллионы лет эволюция не избавилась хотя бы от его части? Какое эволюционное значение имеет то, что у нас он такой большой?
― Сам термин «некодирующий геном» немного устарел. Сегодня мы понимаем, что это та часть генома, которая не кодирует только белки. В то же время существует множество регуляторных не кодирующих белки РНК, которые выполняют не менее важную задачу: регулируют работу определенных генов, в том числе и в процессе клеточной дифференцировки ― превращении клеток из плюрипотентных в специализированные. Исследованием молекулярных механизмов клеточной дифференцировки занимается эпигенетика. Роль регуляторных РНК в работе данных механизмов ― это огромный пласт, который еще не вполне охвачен современной наукой. Возвращаясь к вашему вопросу: ответа на него сегодня нет.
В свое время ученые из США пытались создать хромосому, которая содержала бы только смысловые последовательности, но ничего не получилось: она либо снова набирала множество повторяющихся и других последовательностей, либо попросту выбрасывалась из клеток.
Сегодня мы знаем, как кодируются практически все белки человека. Но это то же самое, что знать, из чего построен дом, и иметь набор кирпичей. А где архитектурный план? Как собирать эти кирпичи? Понятно, что он записан в ДНК, потому что если мы берем ядро и пересаживаем его в пустую яйцеклетку, получается клон ― организм, внешне совершенно неотличимый от исходного. Но то, как именно эта информация закодирована в ДНК, мы совершенно не понимаем. Мы знаем только триплетный код, кодирующий белки, но какие механизмы отвечают за то, что один человек отличается от другого или, например, от мыши, мы не понимаем. Это огромная проблема, решить которую пока очень сложно. Приведу пример: есть заболевание, известное как синдром Тричера Коллинза. Причина его появления ― некое нарушение в работе рибосомных генов, приводящее к тому, что в организме синтезируется меньше рибосом, чем нужно. Казалось бы, дефицит рибосом ― это ведь плохо для всего организма. Но какое фенотипическое проявление мы видим у этого заболевания? Искривленная челюсть. Как это связано с рибосомопатией, о которой я говорил выше? Задача ученых ― разобраться в том, как в генах кодируется фенотип, какие механизмы определяют это. Возвращаясь к вашему вопросу: вполне возможно, что именно эта огромная часть генома, не кодирующая белки, несет данную информацию, просто мы пока не понимаем, как ее расшифровать. Описанная мной ситуация может быть большой проблемой и для генной терапии, о которой сегодня очень много говорят.
Пытаясь вырезать из генома какие-то условно «плохие» гены, мы, сами того не зная, можем выбросить вместе с этим и что-то важное, и это может привести к последствиям, предсказать которые пока сложно.
― Я думала, что вырезают только из тех частей, про которые уже точно все известно.
― Сейчас вообще еще ничего не вырезают, пока это все на уровне разговоров. Но уже сегодня мы можем очень многое сделать в пробирке, в культуре клеток. Так, например, наши эксперименты выявили, что удаление конкретного фермента из раковых клеток укрепляет их ядро и подавляет их способность к миграции, делая их тем самым в значительной мере похожими на здоровые клетки. Это открытие меняет наш взгляд на организацию ядра эукариотической клетки. Согласно традиционному взгляду, знакомому нам еще со школы, ядро представляют вроде некой «коробочки», защищающей ДНК, которая сидит внутри нее. Но на самом деле ядро ― это не «коробочка», а экзоскелет, который формируется вокруг генома! Форма и свойства ядра в значительной мере определяются тем, как упакован геном.
В нашем эксперименте мы, сами того не желая (изначально у нас были другие цели), изменили способ упаковки генома. В результате ядра стали прочными и раковые клетки потеряли свое типичное свойство ― способность мигрировать.
В 2014 г. ученые ИБГ РАН вместе с французскими коллегами показали, что перемещение определенного гена из одной области ядра в другую может активировать его работу не в тех клетках, что требуется. Это запускает комплекс процессов, в конечном итоге приводящих к развитию лейкоза. Фото: rawpixel / 123RF
― Это открытие как-то можно будет применить в медицине?
― Не думаю. Если вы смогли как-то идентифицировать раковую клетку, то лучшее, что с ней можно сделать, ― убить ее, и для этого в медицине уже есть свои эффективные подходы. А лечить такие клетки, в том числе пытаться менять упаковку генома, на мой взгляд, совершенно бессмысленно. Сейчас вся медицина ориентирована на то, чтобы убивать раковые клетки. Поэтому наша работа представляет интерес с точки зрения фундаментальной науки, а не внедрения в клиническую практику.
― Какие из ваших недавних исследований в области 3D-геномики вы считаете наиболее интересными?
― В первую очередь хочу отметить уже упомянутую карту пространственной организации 3D-генома индивидуальных клеток, составленную на основе исследования клеток дрозофил. Эта карта ― самая подробная из имеющихся сегодня карт для индивидуальных клеток. Она обладает разрешением до 10 Кб и до сих пор остается непревзойденной в экспериментах подобного рода.
Очень интересны также наши исследования, касающиеся роли 3D-генома в регуляции работы генов прокариот. Результаты нашей работы в 2025 г. были опубликованы в журнале Nature. Совместно с коллегами из США мы построили карты пространственной организации генома кишечной палочки (Escherichia coli) и увидели ряд новых структур. Так, например, мы впервые показали, что на уровне 3D-генома осуществляется репрессия горизонтально перенесенных генов в клетках (в том числе генов устойчивости к антибиотикам). Это открытие может иметь перспективы для борьбы с антибиотикорезистентностью.
В прошлом году у нас была опубликована еще одна значимая работа. Мы изучили работу 3D-генома амебы диктиостелиум (Dictyostelium discoideum) и показали, что, в отличие от нас, у этого организма никаких ТАД нет. Но есть другая пространственная организация: некие петли, которые тоже могут изолировать одну группу генов от других. Примечательно, что у них есть определенная специализация: очень часто такая петля включает какие-то функционально связанные гены. Видимо, эта необходимость разделять геном на структурно-функциональные домены (ТАД, как у нас, или ограниченные петли, как у амебы диктиостелиум) сложилась на этапе перехода от одноклеточности к многоклеточности. Причем природа делала несколько подобных попыток.
Dictyostelium discoideum интересна тем, что эта амеба может существовать и как примитивный одноклеточный организм, и как более сложное, многоклеточное существо: это происходит тогда, когда многочисленные амебы собираются вместе в какое-то единое тело. Подобные исследования проливают свет на эволюцию и появление многоклеточности на Земле.
Ранее нам еще удалось изучить структурно-функциональные домены в геноме дрозофил. В их геноме тоже есть некие клубки, но они имеют несколько другой механизм образования, нежели ТАД позвоночных животных. Оказалось, что здесь работают самые простые физико-химические законы взаимодействия между отдельными нуклеосомами (элементарными частицами в хроматине ― комплексе белков с ДНК в клеточных ядрах всех эукариот), приводящего к тому, что значительная часть хроматина собирается в глобулу. Эти глобулы разделены участками там, где в силу определенных причин взаимодействие между нуклеосомами невозможно. Это исследование проводилось с помощью суперкомпьютера МГУ им. М.В. Ломоносова «Ломоносов». Как именно происходит описанный мною процесс, показало компьютерное моделирование. Результаты этой работы были опубликованы в журнале Genome Research. Я рассказал лишь о небольшой части наших научных работ. Надеюсь, что в будущем нам удастся провести еще много других интересных экспериментов.