Авторы исследования: Иван Важенин, Елена Герасимова, Егор Уваров, Виталий Ярошенко, Ландыш Фатхутдинова (слева направо).
Фото: Павел Кирильцев / физический факультет университета ИТМО
Простую и быструю технологию синтеза плазмонных* наноалмазов с покрытием из золота и диоксида кремния, предназначенных для лечения меланомы, представили исследователи университета ИТМО в Санкт-Петербурге. Полученные гибридные наноматериалы могут одновременно использоваться для разрушения опухоли с помощью нагревания и измерения температуры тканей. Во время испытаний на лабораторных животных применение наноалмазов позволило замедлить рост злокачественного образования на 65,22%.
Меланома — распространенная разновидность рака кожи. По данным Международного агентства по изучению рака Всемирной организации здравоохранения, в 2022 г. были зарегистрированы 330 тыс. новых случаев заболевания меланомой и 60 тыс. смертей, вызванных этой болезнью.
Один из методов лечения меланомы — гипертермия: локальный нагрев новообразования. Для этого в опухоль вводят специальные наноматериалы, преобразующие энергию света в тепло. В результате светового воздействия на частицы злокачественное образование нагревается до 40–50°C. Под воздействием высокой температуры белки в опухоли разрушаются, и раковые клетки гибнут. Один из материалов, используемых для такой терапии, — наночастицы золота.
Чтобы лечение было максимально эффективным, степень нагревания новообразования должна контролироваться в режиме реального времени, так как от достигаемой температуры зависят механизм экспрессии факторов роста опухоли, метаболизм раковых клеток и вид их смерти. Разновидность клеточной гибели, в свою очередь, определяет, оставят ли уничтоженные клетки продукты распада, способные спровоцировать рецидив болезни.
Для наблюдения за нагревом опухоли используются разнообразные технологии, например, флуоресцентные квантовые точки, а также рамановская или сканирующая зондовая спектроскопия. Но эти подходы не лишены недостатков: так, рамановская спектроскопия и флуоресцентные методы плохо адаптируются к работе с живыми клетками из-за повышенной чувствительности к окружающей среде и фоновым сигналам, а сканирующая зондовая спектроскопия может повредить ткани организма.
Одна из альтернатив, предлагаемых для контроля нагрева раковой опухоли, — флуоресцентные наноалмазы с азото-замещенными вакансиями: один из атомов углерода в кристаллической решетке таких частиц замещен атомом азота. Эти наноструктуры — популярный «инструмент» для термометрии благодаря выгодным свойствам: они биосовместимы, высокочувствительны, обладают оптической стабильностью, не обесцвечиваются под воздействием света и не нуждаются в дополнительной калибровке.
Первый автор исследования, младший научный сотрудник физического факультета ИТМО Елена Николаевна Герасимова.
Фото: Павел Кирильцев / физический факультет университета ИТМО
Что получится, если объединить возможности золотых наночастиц, применяемых для нагрева опухоли, и частиц алмаза, используемых для измерения ее температуры? На этот вопрос с успехом ответили ученые ИТМО, разработав многофункциональный наноматериал, способный одновременно «сжигать» опухоль и измерять ее температуру под воздействием лазера. В основу частиц легли наноалмазы, на которые наносились разные виды покрытия для определения самого удачного сочетания.
Подробнее об испытаниях «Научной России» рассказала первый автор исследования, младший научный сотрудник физического факультета ИТМО Елена Николаевна Герасимова.
«В нашей работе мы использовали наноалмазы как квантовый нанотермометр, а золотая оболочка помогала структуре нагреваться. В процессе исследования мы рассматривали четыре вида наноалмазов: чистые наноалмазы; наноалмазы, покрытые оболочкой из диоксида кремния; наноалмазы, покрытые сплошной золотой оболочкой; а также наноалмазы, покрытые оболочкой из диоксида кремния, на которую нанесена россыпь из золотых наночастиц, — сообщила Е.Н. Герасимова, добавив, что чистые наноалмазы и наноалмазы с прослойкой диоксида кремния использовались как контрольные образцы, так как они не способны нагреваться. — Наноалмазы использовались коммерчески доступные, полученные детонационным путем. Два вида золотой оболочки — сплошная и россыпь золотых наночастиц на прослойке диоксида кремния — были получены химическими методами путем выращивания золота из “семян”».
Применяемая технология позволяет заранее задавать размер наращиваемых на поверхности наноалмазов золотых частиц, что дает возможность регулировать их способность нагреваться.
Мы узнали у исследователя, каким образом наночастицы позволяют измерять температуру опухоли.
Установка для измерения оптически-детектируемого магнитного резонанса.
Фото: Павел Кирильцев / физический факультет университета ИТМО
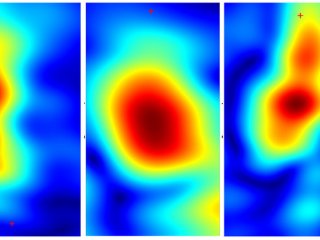
«Для измерения температуры применяются наноалмазы с азото-замещенными вакансиями (NV-центры). NV-центры в алмазах чувствительны к внешней температуре. Ее изменение приводит к деформации кристаллической решетки наноалмаза, в результате чего частота парамагнитного резонанса электрона (ЭПР) NV-центра смещается. Для определения значения частоты ЭПР применяется методика оптически-детектируемого магнитного резонанса (ОДМР), — рассказала Е.Н. Герасимова. — При возбуждении NV-центра лазером с длиной волны 532 нм возникает фотолюминесценция. Если частота микроволнового поля совпадает с резонансной, интенсивность фотолюминесценции уменьшается, потому релаксация электрона происходит через безызлучательный синглетный переход, и, таким образом, в спектре ОДМР будет наблюдаться “провал”. По спектральному сдвигу провала в ОДМР можно рассчитать локальную температуру, в том числе и в клетках».
Сначала действие наноалмазов было испытано на опухолевых клетках и тканях меланомы B16–F10 вне живого организма. Бóльшую эффективность показали «позолоченные» наноалмазы в оболочке из диоксида кремния: при их использовании доля «выживших» раковых клеток составила 51,32%, в то время как для наноалмазов, сплошь покрытых золотом, этот показатель достиг 62,2%.
Далее материал-«победитель» протестировали на лабораторных мышах. Животных разделили на четыре группы: первая не подвергалась терапии, вторую облучали лазером, третьей просто ввели наноалмазы, а четвертая получила наноалмазы в комбинации с лазерным воздействием. Последний подход показал лучший результат в сравнении с отсутствием лечения: рост опухоли у мышей замедлился на 65,22%.
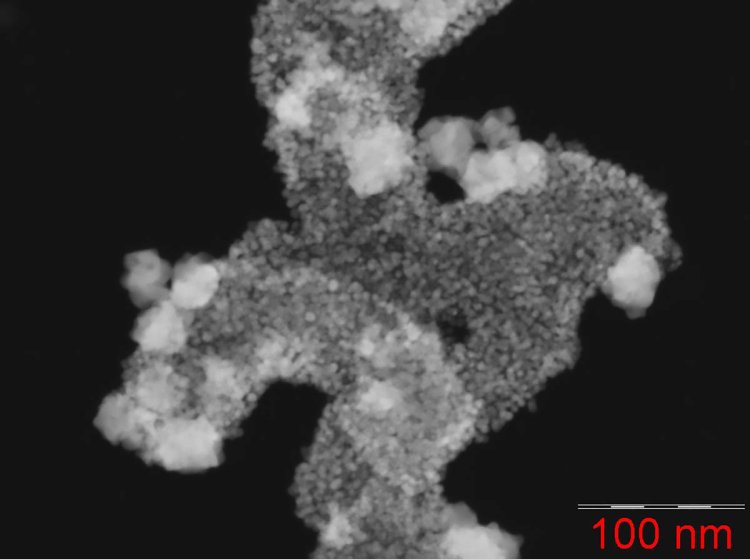
Наноалмазы в оболочке из диоксида кремния, на которую нанесена россыпь из золотых наночастиц, под электронным микроскопом.
Фото: Денис Данилов / ресурсный центр СПбГУ по направлению «Нанотехнологии»
«Для испытания на мыши мы использовали только одну конфигурацию наноалмазов, покрытых россыпью золотых наночастиц на прослойке диоксида кремния. Диоксид кремния позволяет “защитить” алмаз от внешних зарядов, что позволяет измерять ОДМР, — сказала Елена Николаевна Герасимова. — Наноалмазы с россыпью золотых наночастиц были вколоты непосредственно в опухоль в физрастворе в объеме 100 мкл с концентрацией 200 мкг/мл».
Примененный исследователями подход прост, так как для нагревания и измерения температуры опухоли требуется всего один лазер.
«В работе использовался лазер с длиной волны 532 нм (Coherent Obis, 30,66 Вт/см2). Это не оптимальные условия для фототермической терапии, но такая длина волны была выбрана, потому что она соответствует величине, необходимой для возбуждения NV-центров. Опухоль облучалась в течение пяти минут», — отметила Е.Н. Герасимова.
В перспективе созданные в ИТМО наноалмазы можно будет применять для локальной терапии меланомы. В планах исследователей — испытать технологию на бóльшем количестве животных, чтобы уточнить, какие факторы определяют успешность лечения. Кроме того, ученые собираются проверить, как применение алмазных наночастиц сочетается с другими видами онкотерапии.
Подробнее об исследовании можно узнать из статьи в журнале Nanophotonics. Проект реализован при поддержке Российского научного фонда (грант №21-72-30018).
*Плазмонные наночастицы — наноструктуры, состоящие из благородных металлов (обычно золота либо серебра), способные локализовывать электромагнитное поле в масштабах меньших, чем длина волны в оптическом диапазоне. Когда на такие частицы воздействует свет резонансной частоты, на их поверхности начинают коллективно колебаться электроны проводимости, называемые плазмонами. Их колебания крайне чувствительны к окружающим условиям и в зависимости от них меняют свою частоту. Благодаря этому свойству плазмонные наночастицы применяются в различных областях — например, для определения примесей, обнаружения ионов тяжелых металлов, очистки лекарственных препаратов (источник: ИТМО).
Новость подготовлена при поддержке Министерства науки и высшего образования РФ
Фото на превью: Павел Кирильцев / физический факультет университета ИТМО.
Фото на странице: Павел Кирильцев / физический факультет университета ИТМО, Денис Данилов / ресурсный центр СПбГУ по направлению «Нанотехнологии».