Лекарственный препарат ламивудин, который применяют при лечении гепатита B или СПИДа, образует разные связи в кристаллах и в комплексах с белком. При этом с белком ламивудин связывается прочнее, чем с такими же молекулами в кристалле. Полученные данные расширяют представления о механизме действия ламивудина в организме человека и в перспективе могут помочь в разработке новых лекарств против вируса гепатита B и ВИЧ. Результаты исследования, поддержанного грантом Российского научного фонда (РНФ), опубликованы в журнале Biomedicines.
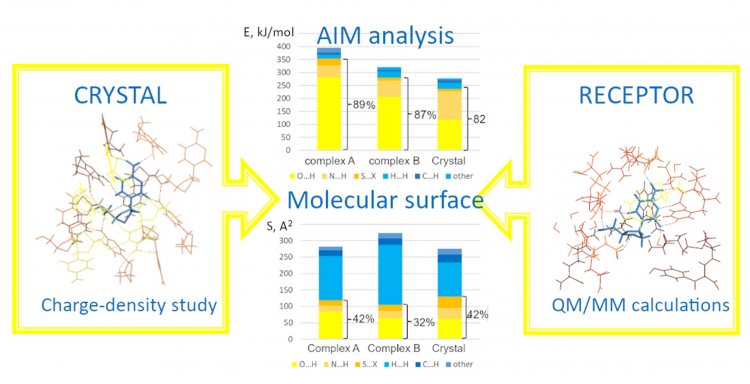
Окружение молекулы ламивудина в кристалле и белковом рецепторе, а также вклады гидрофильных и гидрофобных взаимодействий в величины полной энергии межмолекулярных взаимодействий и площади поверхности молекулы. Источник: Александр Корлюков
Ламивудин — это препарат, который применяют для лечения ВИЧ и гепатита В. Он проникает в человеческую клетку и препятствует работе фермента, который необходим для распространения вируса. При этом этот фермент изначально отсутствует в клетках человека и не выполняет в нашем организме каких-либо функций. В наши клетки он попадает из вируса. Следовательно, препараты, ограничивающие его работу, могут предотвратить распространение вируса. Усовершенствование лекарств требует данных о природе и энергии межмолекулярных взаимодействий, которые формируются как в кристаллической структуре этого лекарства, так и в его комплексах с белками. Эти данные помогают понять, как молекулы из кристалла распределяются по организму человека и как эти молекулы взаимодействуют с белками в клетках. Для сравнения межмолекулярных взаимодействий в разных условиях сегодня анализируют распределение электронной плотности в молекуле.
Ученые из Института элементоорганических соединений имени А.Н. Несмеянова РАН (Москва) совместно с сотрудниками Варшавского университета (Польша) сравнили межмолекулярные взаимодействия ламивудина в кристалле и в комплексах с белками, которые имитировали белковые рецепторы на поверхности клеток человека. Именно с рецепторами связывается ламивудин для проникновения в клетку. Авторы использовали упрощенную модель, которая описывала взаимодействия между цепочками белков и лекарственным препаратом. Эта модель после оптимизации ее геометрии позволила исследователям установить распределение электронной плотности в комплексе молекулы ламивудина с белком. Распределение электронной плотности в кристалле ламивудина ученые установили экспериментально.
С помощью молекулярного моделирования авторы показали, что строение ламивудина зависело от его окружения. То есть в кристаллах и в комплексах с белком молекула имела разную конформацию и образовывала разные межмолекулярные связи. Они характеризуются энергией — чем она выше, тем прочнее связь. При этом независимо от конформации суммарная энергия гидрофобных — «не любящих воду» связей — была одинакова как в кристалле, так и в комплексе. В таких связях участвовала только одна молекула ламивудина, и связи не влияли на прочность связывания ламивудина в кристалле или в комплексе с белком. Иначе вели себя гидрофильные, то есть «любящие воду» части молекул, способные образовывать водородные связи. Эти межмолекулярные взаимодействия формировались между атомом водорода и кислорода или азота. Их суммарная энергия в комплексе с белком была заметно выше, чем в кристалле. В результате общая энергия межмолекулярных взаимодействий в комплексе с белком также оказалась больше. То есть благодаря водородным связям ламивудин прочнее связывался с белком, чем с другими молекулами ламивудина в кристалле. Наиболее значимый вклад приходился на карбоксильные группы, которые входят в состав аминокислот, из которых состоит белок. При этом число водородных связей с участием карбоксильных групп было больше, чем число водородных связей в кристалле, и каждая из них в среднем была прочнее, чем водородные связи между молекулами ламивудина.
Полученные данные необходимы для понимания механизма работы ламивудина. От прочности связей в кристалле зависит, как быстро кристалл ламивудина из лекарственного препарата растворится в нашем организме до молекул. Связи с белком имитируют взаимодействие вещества с рецепторами клетки, силу и прочность связывания с ними. От этого зависят время действия ламивудина и эффективность его проникновения в клетки. Результаты могут способствовать разработке новых лекарственных препаратов на основе ламивудина против ВИЧ и вируса гепатита B.
«Мы надеемся провести еще ряд исследований и получить метод оценки энергий по площади поверхности без сложных расчетов. Кроме того, так как выяснилось, что окружение влияет на типы межмолекулярных связей, мы будем дальше искать закономерности этих взаимодействий», — рассказывает руководитель проекта, поддержанного грантом РНФ, Александр Корлюков, доктор химических наук, ведущий научный сотрудник Института элементоорганических соединений имени А.Н. Несмеянова РАН.
Информация и фото предоставлены пресс-службой Российского научного фонда