Кардиомиопатии — это большая группа заболеваний, которые поражают сердечную мышцу, приводят к сердечной недостаточности и могут повышать риск внезапной смерти. Причиной их возникновения могут стать генетические мутации, а инфекции и вирусы способны усугублять течение заболевания за счет присоединения миокардита. Какие типы кардиомиопатий наиболее распространены среди пациентов? Что первично — кардиомиопатия или миокардит? Как цифровые методы мониторинга помогают врачам Сеченовского университета? Рассказывает кардиолог Юлия Александровна Лутохина.
Юлия Александровна Лутохина — кандидат медицинских наук, доцент кафедры факультетской терапии № 1 Первого Московского государственного медицинского университета им. И.М. Сеченова.
— Юлия Александровна, когда мы беседовали с вами ранее, то рассматривали лишь одну из кардиомиопатий. Как оказалось, их намного больше. Что собой представляет кардиомиопатия и как она влияет на наше сердце?
— Действительно, кардиомиопатии — это многочисленная группа заболеваний, которые объединяет то, что страдает сам миокард, то есть вся сердечная мышца. Причины возникновения кардиомиопатий бывают разные. Но наиболее необычные, на мой взгляд, — это первичные или генетически детерминированные кардиомиопатии.
— Какова связь кардиомиопатий с миокардитами?
— Порой у одного пациента может быть сразу несколько заболеваний миокарда. В частности, могут сочетаться между собой и несколько кардиомиопатий, а также кардиомиопатия и миокардит. Еще десять лет назад подобные случаи считались довольно редкими. А некоторые кардиологи и вовсе считали, что таких сочетаний не может быть. Но если мы сегодня начнем анализировать международные поисковые системы и базы данных по запросу «миокардит и кардиомиопатия», то увидим, что за последние пару лет интерес к этой теме возрос в геометрической прогрессии.
Есть данные, что генетическая основа у пациентов с кардиомиопатией становится причиной присоединения миокардита или вторичного воспаления.
Отмечу, что само присоединение миокардита приводит к ухудшению течения основного заболевания — кардиомиопатии. У пациентов усугубляются нарушения ритма, появляются или прогрессируют симптомы сердечной недостаточности. При этом до сих пор нет единого мнения о том, что считать первопричиной. Одни исследователи полагают, что генетически измененный миокард становится благоприятной мишенью для присоединения воспаления и развития миокардита. Другие, наоборот, уверены, что именно миокардит первичен и способствует реализации аномальной генетической программы, которая, вероятно, без вторичного присоединившегося миокардита могла бы себя не проявить. Как мне кажется, к этому вопросу нужно подходить диалектически. Миокардит и кардиомиопатия представляют собой некий единый континуум, который необходимо анализировать комплексно.
Юлия Александровна работает в кабинете своего учителя — Александра Викторовича Недоступа. Этот кабинет олицетворяет широту и разнообразие интересов выдающегося врача.
«Александр Викторович — учитель каждого доктора, когда-либо работавшего в стенах Факультетской терапевтической клиники. Личность Александра Викторовича невероятно самобытная. Это заметно и по его кабинету, отражающему его разносторонний, богатый внутренний мир».
Фото: Ольга Мерзлякова / «Научная Россия»
«Кабинет Александра Викторовича за несколько лет моей работы в нем еще ни разу не оставил равнодушным ни пациентов, ни коллег. На стенах соседствуют друг с другом выдающиеся врачи, лики святых, летчики-испытатели, священнослужители… Александр Викторович мог часами рассказывать про каждого из людей на портретах и фотографиях. Когда его спрашивали, почему здесь так много разноплановых фотографий и картин, он отвечал, что всех этих людей объединяет высокая духовность». Фото: Ольга Мерзлякова / «Научная Россия»
«Александр Викторович стоял у истоков аритмологии, оставаясь при этом терапевтом широкого профиля. Его работы всегда имели практическую направленность. Все, что изучал Александр Викторович в последующем активно использовалось в клинике. Например, одна из его книг так и называется «Как лечить аритмии». Александр Викторович написал ее в соавторстве с моим наставником Ольгой Владимировной Благовой. На сегодняшний день этот труд выдержал более 10 изданий и остается настольной книгой молодых кардиологов». Фото: Ольга Мерзлякова / «Научная Россия»
«В старинном шкафу табличка с именем Александра Викторовича соседствует с моделями самолетов, космических аппаратов. Это связано с тем, что Александр Викторович стоял у истоков аэрокосмической медицины и активно участвовал в отборе космонавтов и летчиков-испытателей», — отметила Юлия Лутохина. Фото: Ольга Мерзлякова / «Научная Россия»
— Поговорим подробнее о каждом из типов кардиомиопатий. Какова частота их выявления и каковы отличительные черты?
— При различных кардиомиопатиях роль миокардита может отличаться. Начать я бы хотела с аритмогенной кардиомиопатии правого желудочка. Из названия ясно, что чаще всего страдает именно правый желудочек. Хотя бывают и формы с поражением левых камер сердца. При аритмогенной кардиомиопатии миокард замещается жиром и соединительной тканью, а частота миокардита, пожалуй, самая высокая: по нашим данным, более 70%. При аритмогенной кардиомиопатии роль миокардита самая интригующая. Если у пациентов наблюдается латентная аритмическая форма, когда имеются лишь определенные не жизнеугрожающие нарушения ритма, присоединение миокардита можно считать неким триггером.
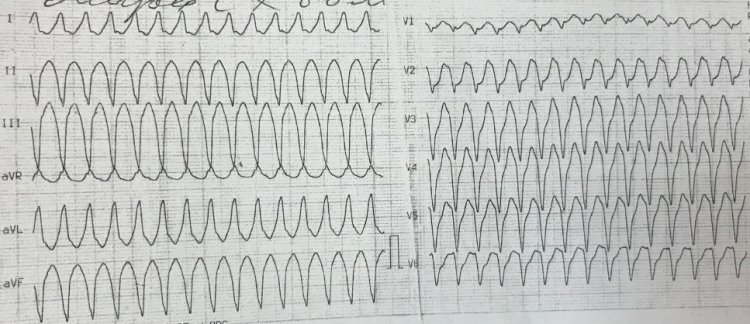
Желудочковая тахикардия у пациентки с аритмогенной кардиомиопатией правого желудочка. Предоставлено Ю.Л. Лутохиной
Есть пациенты с развернутой аритмической формой, у них на первый план выходят нарушения ритма. В этом случае роль миокардита существенно меньше, поскольку генетическая программа уже реализована, и миокардит становится дополнительным фактором. При этой форме частота миокардита будет ниже, порядка 25%.
Существуют еще две формы аритмогенной кардиомиопатии. Одна из них — аритмогенная кардиомиопатия с прогрессирующей сердечной недостаточностью, при которой у пациентов наблюдаются одышка, снижение переносимости физических нагрузок. Последняя форма — особая. Речь идет о сочетании аритмогенной кардиомиопатии и некомпактного миокарда. При этих двух формах частота миокардита превышает 85%, а его вклад в развитие болезни крайне существенен.
Работая с пациентами с аритмогенной кардиомиопатией, мы боремся с основной проблемой — аритмиями, но при этом всегда помним о возможном присоединении миокардита. Вовремя отследить это помогают специальные исследования, результаты которых либо подтверждают его наличие, либо исключают.
В случае если миокардит все-таки обнаружен, мы меняем тактику лечения пациента и уделяем внимание не только основному заболеванию —аритмогенной кардиомиопатии, но и сопутствующему миокардиту.
Нам впервые удалось продемонстрировать, что лечение сопутствующего миокардита у пациентов с аритмогенной кардиомиопатией снижает смертность, улучшает эффект от антиаритмической терапии. Поэтому важно не только диагностировать миокардит, но и не игнорировать его в рамках терапии.
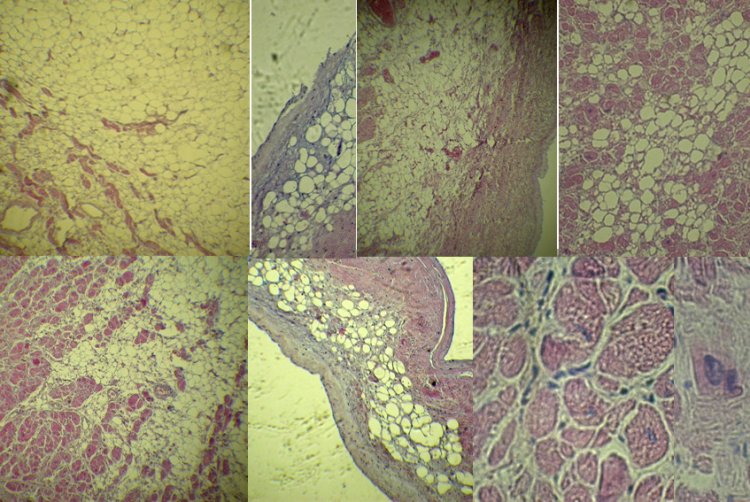
Гистологическое исследование сердца у пациентки с аритмогенной кардиомиопатией правого желудочка. Более 70% жизнеспособного миокарда замещено жиром и соединительной тканью. Предоставлено Ю.Л. Лутохиной
— Насколько значимой может быть постоянная диагностика миокардита?
— На самом деле постоянная диагностика не имеет смысла. Это экономически нецелесообразно как минимум. Но когда пациенты приходят на контроль, а такие пациенты появляются в нашем поле зрения не реже, чем один раз в год, то наряду с обычной эхокардиографией, ЭКГ и холтеровским мониторированием мы производим своего рода скрининговый анализ крови. Он и позволяет нам судить о наличии активности миокардита.
— Миокардит при кардиомиопатиях особенный? Чем он отличается от миокардита без кардиомиопатий?
— Миокардит при кардиомиопатиях различен. Он может иметь первичную природу, когда пациент проконтактировал с неким вирусом или инфекцией. При выработке антител для борьбы с вирусом антитела остаются в организме. Казалось бы, какое отношение базовые процессы иммунного ответа имеют к миокардиту? Дело в том, что у некоторых пациентов антигены миокарда оказываются похожими на антигены вируса или бактерии. Поэтому вскоре антитела, которые организм добросовестно синтезировал для борьбы с вирусной инфекцией, начинают атаковать собственный миокард пациента. На этом фоне возникает развитие воспаления со всеми вытекающими последствиями.
Существует также вторичный миокардит при кардиомиопатиях, который имеет аутоиммунную природу. Генетически измененный миокард становится благоприятной мишенью для аутоиммунной агрессии организма. Например, при аритмогенной кардиомиопатии, когда мы анализируем, на каких структурах миокарда откладываются антитела, отчетливо видим, что они зачастую расположены в области вставочных дисков, которые как раз поражаются при аритмогенной кардиомиопатии.
— То есть необходимо отслеживать иммунные реакции?
— Мы не можем проконтролировать какие-то иммунные биомаркеры, которые бы позволили нам точно сказать о наличии миокардита или о том, что определенные звенья иммунной системы работают неправильно. Но по косвенным данным мы можем судить о наличии аутоиммунной агрессии, когда фиксируем антитела к каким-то структурам миокарда — ядрам, кардиомиоцитам, проводящей системе или вставочным дискам.
— Расскажите о миокардите при некомпактном миокарде левого желудочка.
— Некомпактный миокард — довольно распространенная кардиомиопатия. Ее частота в зависимости от популяции (среди взрослых и детей) в среднем варьирует от одного пациента на 500 человек. Речь идет об особой структуре некомпактного слоя миокарда. В норме у здорового человека миокард состоит только из компактного слоя. При патологии присутствует еще один — некомпактный, который похож на сеточку. Пациенты в большей степени подвержены развитию сердечной недостаточности, поскольку некомпактный слой мешает адекватной сократимости миокарда. Сетчатая, губчатая структура миокарда может стать предпосылкой также для формирования тромбов, что увеличивает риск тромбоэмболических осложнений по сравнению с общей популяцией.
И, конечно, подобная генетическая кардиомиопатия становится причиной присоединения миокардита. По данным регистра, который ведут коллеги, частота миокардита в нашей выборке пациентов составляет 50–53%. И что особенно важно — миокардит вносит вклад в развитие болезни. Пациенты, у которых некомпактный миокард сочетается с миокардитом, конечно, клинически тяжелее.
К счастью, на фоне иммуносупрессивной терапии миокардита наблюдается улучшение сократимости миокарда и уменьшение выраженности нарушений ритма.
— Вы упомянули детей. Насколько часто у них диагностируют кардиомиопатии?
— Напомню, что кардиомиопатия напрямую связана с генетикой, поэтому частота заболевания среди взрослых и детей не различается. Как правило, такие пациенты вырастают и приходят к нам из педиатрии, где они наблюдаются, с 18 лет.
С другой стороны, некоторые кардиомиопатии дебютируют в более позднем возрасте. То есть ребенок может быть носителем патогенной мутации, но сами признаки кардиомиопатии могут проявиться у человека в зрелости. Среди наших пациентов были те, у которых диагноз «кардиомиопатия» мы ставили после 60 и даже ближе к 70 годам. Конечно, первые симптомы появились раньше, просто их расценивали как проявление других, более частых и более очевидных заболеваний сердца.
— Перейдем к другому типу кардиомиопатий — гипертрофической. Расскажите, какова ее частота и как она себя проявляет?
— Гипертрофическая кардиомиопатия тоже достаточно часто встречается в популяции (порядка одного пациента на 500 человек). В этом случае миокард утолщен, гипертрофирован. Ранее я отмечала, что миокард — это такая же мышца, как и другие в организме. Поэтому он так же может реагировать на нагрузку. Думаю, многие люди видели у себя в заключении по кардиограмме «признаки гипертрофии миокарда». Как правило, это гипертоники, у которых сердце справляется с повышенной нагрузкой, по сути с повышенным кровяным давлением. Кроме того, среди пациентов с гипертрофией миокарда встречаются профессиональные спортсмены.
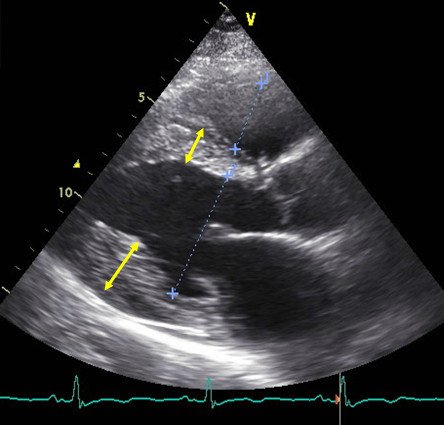
Выраженная гипертрофия (утолщение) миокарда по данным эхокардиографии (УЗИ сердца) у пациента с гипертрофической кардиомиопатией (желтые стрелки). Предоставлено Ю.Л. Лутохиной
Но в отличие от просто гипертрофии миокарда гипертрофическая кардиомиопатия сопровождается более выраженным утолщением миокарда и представляет собой серьезное заболевание, которое имеет под собой генетическую основу. Для пациента это чревато различными нарушениями ритма, причем иногда жизнеугрожающими, как и при аритмогенной кардиомиопатии, вплоть до внезапной сердечной смерти.
У пациентов с гипертрофической кардиомиопатией толстый миокард может постепенно замещаться соединительной тканью. Со временем камеры сердца могут расширяться, сократимость снижаться, что становится причиной развития сердечной недостаточности и, как следствие, ухудшения состояния больного.
Тем не менее у таких пациентов миокардит мы видим реже. В нашем регистре пациентов с гипертрофической кардиомиопатией его частота составляет порядка 30%. Сегодня мы с коллегами как раз исследуем эффективность лечения миокардита у этой группы пациентов, поскольку данных по этому вопросу нет.
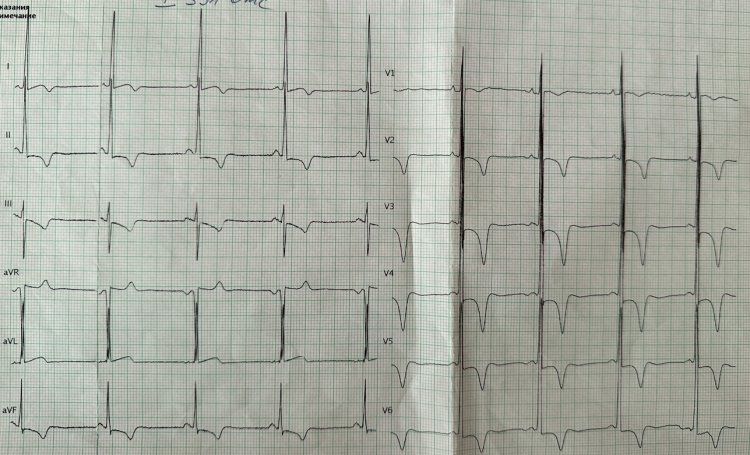
Признаки гипертрофии миокарда у пациента с гипертрофической кардиомиопатией (высокий вольтаж). Предоставлено Ю.Л. Лутохиной
— Расскажите об особенностях другого типа кардиомиопатий, а именно о дилатационной кардиомиопатии. В чем ее особенности?
— Дилатационная кардиомиопатия — пожалуй, один из самых неоднозначных диагнозов у пациентов. Когда пациент обращается с диагнозом ДКМП как окончательным, для врача это повод задуматься о причинах. Под дилатационной кардиомиопатией в широком смысле понимают расширение сердца. В литературе часто используют название «бычье сердце». Природа патологии может быть разная. Дилатация сердца нередко становится следствием миокардита.
К сожалению, очень часто этот диагноз в первичном звене становится финальным. Врач устанавливает наличие дилатационной кардиомиопатии, назначает лечение и настраивает пациента на то, что вскоре ему предстоит трансплантация сердца.
Если говорить о первичной, генетически детерминированной кардиомиопатии, то в этом случае дилатация вызвана определенными мутациями. Есть данные, что некоторые кардиотропные вирусы из-за мутаций лучше фиксируются к кардиомиоцитам и быстро распространяются по миокарду, что приводит к вторичному воспалению. То есть первичная генетика влияет на развитие воспаления и присоединение миокардита.
Поэтому, когда к нам обращается пациент с дилатационной кардиомиопатией, мы рассматриваем диагноз как синдром и очень тщательно подходим к нозологической диагностике. Необходимо четко знать, что стоит за диагнозом: миокардит, вызвавший дилатацию камер сердца, или же генетика, исходно приведшая к патологии и присоединению миокардита.
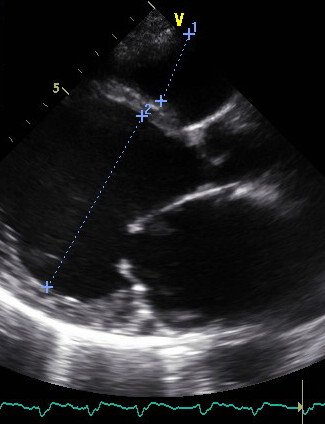
Расширение камер сердца при эхокардиографии (УЗИ сердца) у пациентки с дилатационной кардиомиопатией. Предоставлено Ю.Л. Лутохиной
Мы активно изучаем этих пациентов. И мой научный руководитель Ольга Владимировна Благова написала очень много интереснейших работ на эту тему, в том числе о природе ДКМП, установке нозологического диагноза и подходах к лечению. Поэтому в нашей клинике мы активно занимаемся пациентами с так называемыми большими сердцами. И, к счастью, иногда есть возможность побороться за здоровье больных и избежать трансплантации сердца.
— Поговорим о рестриктивной кардиомиопатии. В чем ее особенности?
— Рестриктивная кардиомиопатия — самая редкая из всех кардиомиопатий. Она характеризуется тем, что сердце не может нормально расслабляться. В основном все следят за тем, чтобы сердце хорошо сокращалось, качало, функционировало. И при других кардиомиопатиях ухудшается именно сократительная функция. При рестриктивной кардиомиопатии сердце сокращается хорошо, а расслабление миокарда, напротив, нарушено, поскольку миокард вдруг становится жестким.
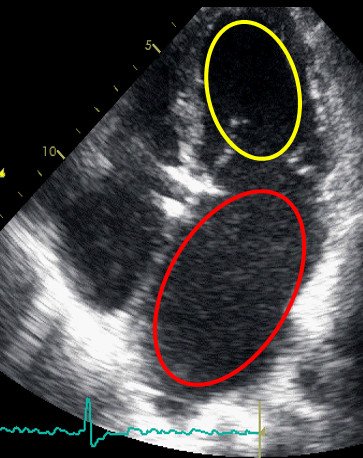
Эхокардиография (УЗИ сердца) пациента с рестриктивной кардиомиопатией значительно увеличено левое предсердие (красный цвет) при нормальных размерах левого желудочка (желтый цвет). Предоставлено Ю.Л. Лутохиной
Первичная рестриктивная кардиомиопатия также связана с мутациями, которые приводят к изменению миокарда. Но причиной могут стать и болезни накопления, например гемахроматоз, при котором в миокарде накапливается железо, или амилоидоз сердца, вызванный патологическим фибриллярным белком. Кардиомиоциты наполняются аномальным белком, и миокард не может нормально расслабляться. У таких пациентов развивается тяжелая сердечная недостаточность, появляются нарушения ритма.
Сегодня мы работаем над методами диагностики миокардита у пациентов с рестриктивной кардиомиопатией и, конечно, разрабатываем подходы к лечению таких пациентов.
— Подведем итог нашей беседы о кардиомиопатиях. Насколько эффективны существующие подходы к лечению пациентов с разными видами заболеваний?
— Конечно, у нас нет универсального подхода для каждого из видов кардиомиопатий. Но в целом наиболее важным аспектом, объединяющим все описанные патологии, становится ранняя диагностика.
Отмечу, что диагностирование определенной кардиомиопатии накладывает некие обязательства на самого пациента с точки зрения изменения образа жизни. Например, есть те кардиомиопатии, которые не приемлют чрезмерных физических нагрузок. В том или ином случае мы назначаем разные типы препаратов, которые, например, замедляют замещение миокарда фиброзно-жировой тканью.
Что касается непосредственно генетической основы, то скажу прямо: пока мы ничего не можем сделать. По научным публикациям мы видим, что ведутся активные поиски в направлении разработки эпигенетической терапии для аритмогенной и гипертрофической кардиомиопатий, которая позволяет замедлить развитие заболевания у лабораторных животных. Мы очень надеемся, что в будущем подобные решения перейдут в практику.
— Один из симптомов кардиомиопатий, который вы не раз упомянули, — это сердечная недостаточность. Насколько мне известно, в Сеченовском университете появился проект цифрового мониторинга таких пациентов. Расскажите об этом.
— Сердечная недостаточность как синдром развивается у пациентов с самыми разными заболеваниями сердца — не только при кардиомиопатиях, но и при гипертонической и ишемической болезнях сердца. Как она себя проявляет? В первую очередь это одышка, снижение переносимости физических нагрузок, отеки, слабость, утомляемость.
Несмотря на то что сердечную недостаточность ставят достаточно часто и отношение к этому диагнозу среди пациентов более-менее спокойное, все-таки это довольно тяжелый синдром, который сопровождается неблагоприятным прогнозом при кажущемся благополучии. Поэтому таких пациентов нужно активно лечить и по возможности предотвращать декомпенсации. Если ничего с этим не делать, то рано или поздно пациент придет к состоянию, когда он просто не сможет нормально жить без госпитализаций. Он будет вынужден периодически ложиться в стационар для лечения. Причем чем дольше сердечная недостаточность протекает без внимания, тем чаще пациенты нуждаются в госпитализациях, что негативно влияет на качество жизни.
Поэтому очень важно отслеживать пациентов с сердечной недостаточностью и своевременно выявлять самые ранние признаки декомпенсации. Современные фармакологические возможности в лечении сердечной недостаточности позволяют достаточно успешно с ней справляться и решать те или иные проблемы без госпитализации.
В этом году мы выиграли финансовую поддержку для создания Инновационной научной школы под руководством академика Ю.Н. Беленкова и заведующего нашей кафедрой члена-корреспондента РАН В.В Фомина. В этой школе мы используем разработанный коллегами на кафедре госпитальной терапии № 1 телеграм-бот, который помогает осуществлять мониторинг пациентов с сердечной недостаточностью самой разной этиологии. Телеграм-бот позволяет нам наблюдать за пациентами совершенно неинвазивно. Пациенту ежедневно поступает определенный набор вопросов. В зависимости от того, как больной отвечает на вопросы, можно оценить его состояние. Это эффективный и важный инструмент, поскольку больных с сердечной недостаточностью очень много. Отследить каждого больного даже на этапе первичного звена, в поликлинике, практически невозможно. Это колоссальная нагрузка на систему здравоохранения. Поэтому подобная автоматизация процесса и помогает самим пациентам, которые ощущают поддержку и связь с врачом, и существенно снижает нагрузку на медицинский персонал в первичном звене.
Проект сейчас активно развивается. Мы продолжим анализировать результаты, а также расширять группы пациентов, нуждающихся в особо тщательном мониторинге. Хочется вспомнить о моем наставнике Александре Викторовиче Недоступе, который огромное внимание уделял тому, чтобы достижения науки имели практическую направленность. Мы продолжаем эту линию и очень надеемся, что наши исследования, публикации в научных журналах в будущем принесут практическую пользу. Ведь в конечном счете все это делается для наших пациентов, для их блага.