Синтетическая биология позволяет создавать новые организмы с заданными свойствами. И если классическая генная инженерия — это редактирование уже существующей книги жизни, то синтетическая биология — это попытка написать свою собственную с чистого листа. Пока подобные технологии применяют в основном к бактериям и другим примитивным существам, но каковы их будущие перспективы и и возможности? Какие организмы ученые умеют создавать с нуля уже сейчас? С какими трудностями сталкиваются специалисты, работающие в этой области знания, и о чем они мечтают? Об этом — наш разговор с биологом Евгением Максимовым.
Справка: Евгений Георгиевич Максимов — доктор биологических наук, заведующий лабораторией физико-химии биомембран биологического факультета МГУ им. М.В. Ломоносова, координатор научно-образовательной школы МГУ «Молекулярные технологии живых систем и синтетическая биология», член Координационного совета по делам молодежи в научной и образовательной сферах Совета при Президенте РФ по науке и образованию, лауреат премии правительства Москвы для молодых ученых. Автор более 150 научных публикаций.
— Что такое синтетическая биология и чем она отличается, например, от генной инженерии?
— Синтетическая биология — область молекулярной биофизики, объединяющая возможности генной инженерии, физики белка, структурной биологии для создания новых уникальных инструментов. Это позволяет получать не встречающиеся в природе биологические объекты на основе строительных блоков, которые можно синтезировать с помощью методов химического и органического синтеза, либо на основе имеющихся в нашем распоряжении природных строительных блоков. Полученные объекты могут обладать новыми необычными полезными свойствами, поэтому синтетическая биология представляет очень большой интерес для ученых. Что касается отличия от генной инженерии, то синтетическая биология использует ее методы. Это смежные дисциплины, которые не могут существовать друг без друга.
— Мне на память приходят громкие эксперименты последних десятилетий: выведение зеленых светящихся поросят, генетические манипуляции с козами, которых «научили» давать белок, образующий паутину, и прочие. Но в данном случае речь идет о модификации уже существующих животных, а что самое сложное удалось создать сегодня с нуля с помощью методов синтетической биологии?
— Давайте вспомним Нобелевскую премию 2024 г. по химии, которая была присуждена за разработку методов, позволяющих предсказывать структуру белков, используя искусственный интеллект и нейросети. Эти открытия, с одной стороны, решают извечную проблему, каким образом могут выглядеть белки, если известна только последовательность аминокислот, а с другой стороны, позволяют предсказать и некоторые важные структурные и функциональные свойства этих белков. Пожалуй, именно это направление синтетической биологии можно назвать сегодня самым значимым и быстро развивающимся. Многое в этой области было сделано благодаря предыдущим открытиям структурной биологии, но именно экспериментальное определение структуры белка позволило понять, как устроены белки, из чего они состоят, с какими группами взаимодействуют. Понимание физики этих взаимодействий позволяет делать предсказания с очень большой точностью, на уровне 90%.
Методы, отмеченные Нобелевской премией в 2024 г., по сути, опираются на базы данных, включающих огромное количество последовательностей, структур, полученных экспериментально. Они статистически предсказывают, какими свойствами и структурой могут обладать не существующие в природе белки, созданные на основе схожих аминокислотных последовательностей. Но здесь есть одна проблема. То, что предсказывает модель, всегда остается некой теорией. И то, каким будет тот или иной объект в реальности, может показать только эксперимент.
Второй важный момент: сегодня у ученых есть возможность синтезировать бесконечное множество различных аминокислот для получения новых белков, но предсказывать такие новые структуры нейросети пока не могут.
Исследования, отмеченные Нобелевской премией по химии 2024 г., вывели на новый уровень качество предсказания структуры белков (программа AlphaFold) и позволили создавать с помощью компьютера новые белки, которых нет в природе (с участием программы Rosetta).
Изображение: Niklas Elmehed / Nobel Prize Outreach
― То есть они предсказывают, какими будут белки, построенные из стандартных 20 аминокислот, которые отвечают за синтез белков во всех живых организмах, но не из других аминокислот?
― Да. Когда химическая структура заместителей в этих аминокислотах отличается от природных типов и, соответственно, не встречается в белках, чья структура известна и депонирована в соответствующей базе данных, это становится проблемой. Тем временем подобные аминокислоты довольно легко синтезировать и у ученых есть много методов, позволяющих строить белки с новыми интересными свойствами из таких необычных аминокислот.
По сути, это новая биохимия, и уровень сложности, который можно внести в белковые структуры, здесь значительно выше по сравнению с тем, что дает базовый набор аминокислот.
― Эти новые аминокислоты выходят за базовый набор из 20, но все же существуют в природе? Или речь о том, что можно создать принципиально иные, не встречавшиеся нигде аминокислоты?
― Речь о так называемых неканонических аминокислотах. Они существуют в природе, но выходят за базовой набор протеиногенных аминокислот. Новизна здесь заключается в том, что мы можем по-разному их комбинировать. Примечательно, что многие из этих аминокислот прилетают к нам из космоса. Генетический код на нашей планете таков, что эти аминокислоты здесь не используются: видимо, они были слишком редкими или не столь необходимыми. Но это не значит, что они не могут быть востребованными на других планетах.
― А наши, наоборот, будут ненужными.
― Да. Это некая особенность, связанная с начальными условиями развития жизни на планете.
― Для чего нужны белки, созданные с помощью таких неканонических аминокислот?
― Это позволяет модифицировать структуру белков очень тонким образом, например производить замены аминокислот которые принято называть мутациями, но в данном случае это скорее хирургия на уровне отдельных атомов. Такие манипуляции позволяют лучше понять принципы работы белков, изучить, что происходит в них при взаимодействии с какими-то кофакторами или с другими белками. В то же время это дает возможность вносить новые свойства в белки: например, можно абсолютно уникальным и селективным образом пометить необходимый белок и наблюдать за его активностью в клетке или в организме. Можно также создать новый белок, который будет осуществлять какую-то уникальную химическую реакцию, например катализ.
― Подобные белки уже пробовали внедрять в живые организмы?
― Да, это возможно. Более того, есть возможность модифицировать генетический код простейших микроорганизмов, что позволяет освободить определенные кодоны в генетическом коде под использование их для неканонических аминокислот. Это сложная, но очень важная задача ― управлять тем, как жизнь использует генетический код и аминокислоты, составляющие основу белков.
― А если говорить не об отдельных белках, а о создании целых клеток и организмов с заданными свойствами с нуля, то какие главные препятствия здесь существует?
― Прогресс в этой области ушел далеко вперед. Есть созданные с нуля синтетические организмы, например микоплазма, чей генетический код был значительно отредактирован. Интересное свойство таких организмов заключается в том, что они совершенно невосприимчивы к вирусам. Вирус пытается воспользоваться их генетическим кодом, но он неспособен генерировать генетическую последовательность и в дальнейшем белки, необходимые ему для воспроизводства. Таким образом, этот вирус просто не может себя копировать.
Подобные синтетические организмы зависимы от ресурсов, необходимых им для роста и жизни, то есть без неканонических кислот они обойтись не могут, и, соответственно, обитать такие «существа» способны только в условиях лаборатории.
Создание невосприимчивых к вирусам организмов можно назвать задачей двойного назначения. Потенциально геном человека тоже можно отредактировать таким образом, что он будет невосприимчив к вирусам. А теперь представьте, что какая-то страна, с одной стороны, сделала свою популяцию устойчивой к вирусам, с другой ― создала вирус, который может убить всех. Поэтому в области синтетической биологии есть множество этических проблем. До каких пределов мы можем редактировать жизнь? Можно ли менять основу генетического кода и создавать какие-то новые организмы? Как эти новые организмы будут взаимодействовать с природными сообществами? Эти вопросы ждут ответов. Мы же, в свою очередь, занимаемся не философскими вопросами, а гражданскими научными исследованиями, результаты которых призваны сделать жизнь человека лучше.
― В прошлом году у меня вышло интервью с биологом Петром Каменским. Рассказывая о синтетической биологии, он говорил, что у ученых есть большой интерес к тому, чтобы превратить бактерии в некие биофабрики, которые можно будет использовать для наработки больших количеств полезных продуктов. Можно сказать, тотальное порабощение бактерий! Что вы думаете об этом?
― Да, такие работы существуют. В распоряжении ученых есть широко используемый и универсальный подход, при котором бактерию ставят перед выбором: либо она синтезирует нужный белок, либо погибает. Если она решает синтезировать белок, то за счет определенного набора генов (которые она синтезирует вместе с целевым рекомбинантным белком) бактерия приобретает устойчивость к антибиотику.
― А в природе бактерии не всегда синтезируют нужные нам вещества?
― В природе они вообще никогда этого не делают.
― То есть могут, но не хотят?
― Им это просто невыгодно энергетически. Если это не вопрос выживания, то зачем тратить энергию? Именно поэтому в лабораторных условиях, чтобы получить необходимые белки, бактерию ставят перед жизненно важным выбором.
― При этом желательно, чтобы это была какая-то большая популяция бактерий, чтобы эффект был ощутимым?
― Да. Как правило, для получения миллиграммов белка требуются литры культур бактерий, то есть миллиарды и триллионы бактериальных клеток!
― Я знаю, что для вас синтетическая биология ― самое интересное научное направление. Над чем вы сейчас работаете?
― В первую очередь над созданием новых флуоресцентных и фотоуправляемых белков. Методы синтетической биологии позволяют использовать неканонические аминокислоты, о которых мы говорили выше. Мы столкнулись с ограниченностью природного набора аминокислот, исследуя, как работает фотоактивный оранжевый каротиноидный белок (Orange Carotenoid Protein, OCP). В природе он нужен для защиты цианобактерий от фотоповреждения. При очень ярком свете он может переходить из неактивного состояния в активное, но делает это неохотно, поскольку в природе этой реакции препятствует наличие нескольких контактов между белком и каротиноидом. Мы пытались модифицировать данные контакты таким образом, чтобы оставить только один, повысив тем самым выход фотопродукта. Это открывает возможности для изучения фотопереключения и сопутствующих этому процессу реакций.
По сути, мы перебрали все возможные варианты природных аминокислот, и оказалось, что сделать это можно было только с помощью неканонических. Этот новый метод мне очень понравился, и я понял, что он пока мало где используется, а перспектив у него достаточно много. Благодаря этой работе мы решили создать новую лабораторию, специализирующуюся на подобных методах и подходах.
Сотрудники лаборатории создали уникальную установку на основе фемтосекундного лазера и детекторов единичных фотонов, позволяющую измерять кинетику затухания флуоресценции и получать изображения (Fluorescence Lifetime Imaging Microscopy, FLIM). Видео: Александр Козлов / «Научная Россия»
― Какие еще организмы, помимо цианобактерий, вам интересны?
― Мы работаем с зелеными водорослями, человеческими клетками и даже с целыми организмами (некоторые эксперименты проводятся на лабораторных животных: мышах, крысах и кроликах). Это совместная работа, в которой нам помогают коллеги из ФИЦ «Фундаментальные основы биотехнологий» РАН, ИБХ РАН, МФТИ, ИФР РАН и других научных центров, имеющие необходимые оборудование и компетенции. В наши задачи входит изучение функциональных свойств белков. Нам интересно исследовать то, как одни белки взаимодействуют с другими, как они проникают в клетки, что они там делают и т.д. Если в процессе работы мы понимаем, что белок может иметь какую-то пользу для медицины, то начинаем задумываться об экспериментах с участием животных.
― Выше мы говорили о бактериях. А насколько проблематично создать что-то более сложное, например эукариотическую клетку, у которой, в отличие от бактерий, есть ядро?
― Пожалуй, это очень сложно по многим причинам. Самая очевидная из них ― размеры. Геном прокариот (одноклеточных организмов, не имеющих клеточного ядра и других внутриклеточных органелл. ― Примеч. корр.) намного меньше, чем у эукариот. Создание с нуля полностью синтетической эукариотической клетки, не говоря уже о целом организме, может быть крайне непростой задачей. Тем не менее ученые занимаются этим, и я не сомневаюсь, что рано или поздно цель будет достигнута.
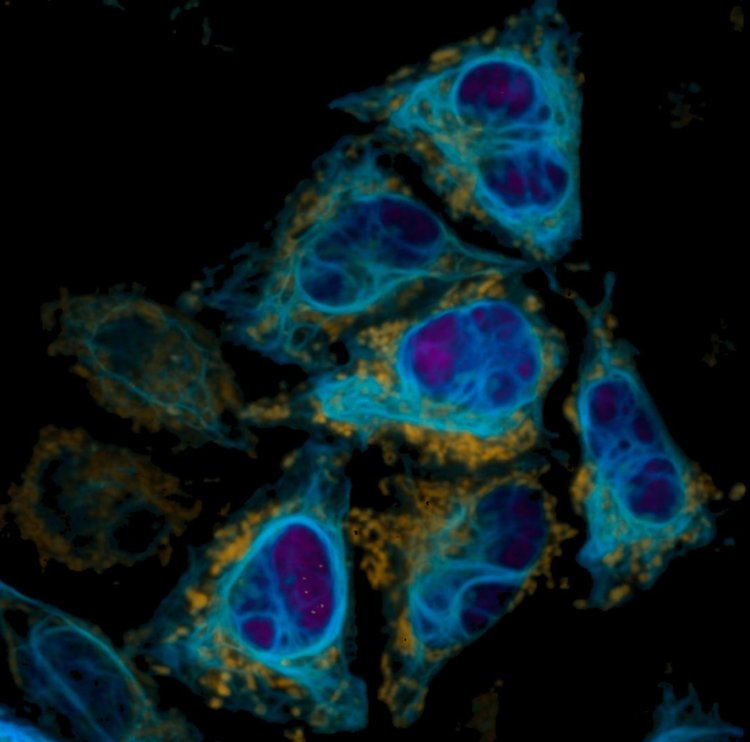
Пример FLIM-изображения человеческих раковых клеток HeLa, экспрессирующих варианты белков FAST с локализациями в различных органоидах. Изображение: Евгений Максимов / МГУ
― Правда ли, что одним из самых больших препятствий в этой области остается создание клеточной мембраны?
― Да, это имеет принципиальное значение. Мембраны были и остаются неким природным барьером между внешней и внутренней средами клетки. На мембранах находится огромное количество белков, участвующих в регуляции метаболических реакций. Изучение того, как клетки взаимодействуют с окружающим миром и передают сигналы друг другу, как они отвечают на полученные сигналы, ― одна из важных задач нашей лаборатории.
― Могут ли в будущем синтетические организмы заменить исчезнувшие из природных экосистем организмы?
― Можно пофантазировать и представить, что синтетические организмы, адаптированные под определенные условия среды, вполне могут быть использованы, например, для терраформирования Марса и других планет. Здесь, как мне кажется, многое зависит от конкретной задачи и понимания условий, сложившихся в данный момент. Приведу другой пример. Если где-нибудь происходит разлив нефти, то на помощь могут прийти организмы, которые умеют перерабатывать эту нефть, хотя подобные условия обитания для них нехарактерны. Их нужно найти и выделить в чистую культуру. Этим занимаются микробиологи, которые часто помогают предприятиям в борьбе с последствиями экологических бедствий.
― А захотят ли эти организмы есть нефть? Вдруг на месте аварии и в его окрестностях найдется что-нибудь повкуснее?
― Такое тоже возможно. В целом всегда, когда есть выбор, жизнь будет выбирать более легкий путь. Поэтому если эта нефть представляет собой какой-то уникальный, единственный субстрат, тогда, конечно, микробы будут перерабатывать в первую очередь именно ее. Разливы нефти могут происходить повсюду, в том числе в северных регионах. Тем не менее даже там ученые находят бактерии, которые могут питаться этой нефтью, устраняя загрязнения.
― В группе вашей лаборатории в Telegram был пост о трех ваших научных мечтах: снять настоящее молекулярное кино, собрать белок, полностью состоящий из неканонических аминокислот, и измерить температуру в разных частях клетки. Вам удалось приблизиться к своим целям?
― Я пытаюсь мечтать по-крупному. Если говорить о молекулярном кино, то мы все очень ждем, когда в России заработает синхротрон СКИФ. Эта мегасайенс-установка позволит проводить структурные эксперименты с временны́м разрешением. Это означает, что, используя короткую вспышку света, можно будет запустить какую-то фотохимическую реакцию, а затем посмотреть через определенный промежуток времени, как изменилась структура белка, и сравнить с тем, что было в начале. Пожалуй, термин «молекулярное кино» ― некое преувеличение, но набор из нескольких подобных кадров может быть очень полезен для понимания того, как работает фотопереключаемый белок или какая-то фотоуправляемая система.
Что касается создания белка на основе неканонических аминокислот, то мы работаем в этом направлении.
На текущий момент мы можем успешно вводить одну неканоническую аминокислоту, и это уже открывает перед нами много новых возможностей для модификации белка и изучения его свойств.
Если же мы научимся вводить три-четыре неканонические аминокислоты, то это будет еще интереснее, потому что даст возможность решать другой класс проблем, в том числе связанных с организацией уникальных каталитических центров.
Сотрудники лаборатории физико-химии биомембран биологического факультета МГУ. Слева направо: Иван Прохоров, Евгений Максимов, Светлана Сидоренко. Фото: Ольга Мерзлякова / «Научная Россия»
Отвечая на вопрос об измерении температуры клетки: здесь есть давняя биофизическая проблема, связанная с тем, что любые реакции, сопровождающиеся выделением тепла, влияют на температуру в ближайшем окружении. Расчеты показывают, что это могут быть довольно большие изменения температуры. В клетках теплокровных животных, например, могут наблюдаться особенно высокие градиенты температуры в районе митохондрий. Это связано с тем, что там активно протекают метаболические реакции. Наверняка эта температура должна отражать активность органелл и метаболизма в целом.
Поэтому иметь инструменты, которые бы позволяли измерять температуру локально, было бы очень полезно для изучения клеток и того, как они себя чувствуют в разных условиях. Думаю, это самая технически простая задача из трех перечисленных и она обязательно будет решена в будущем.
― Прибавились ли какие-то новые мечты к этим трем за последнее время?
― Я очень хочу, чтобы мои студенты, аспиранты и сотрудники научились хорошо писать статьи, заявки на гранты, получали премии. Это моя задача как заведующего лаборатории ― подготовить молодых сотрудников к самостоятельной работе.