Трансплантация костного мозга позволила человечеству серьезно продвинуться в борьбе с онкологическими и врожденными заболеваниями, а новейшие исследования — существенно расширить возможности применения такого метода лечения. Однако серьезными препятствиями тому, чтобы сделать пересадку костного мозга общедоступной опцией, по-прежнему становятся неосведомленность, а зачастую и вовсе ложные представления об этой процедуре со стороны потенциальных доноров. «Научная Россия» объясняет, что такое трансплантация костного мозга в действительности и о чем говорят исследования в этой области.
Сам метод трансплантации костного мозга известен с середины ХХ в., в СССР первая такая операция была проведена в 1985 г. Это если говорить о пересадке стволовых клеток в современном понимании; а вообще возможности костного мозга интересовали ученых с конца XIX в.: соответствующие эксперименты, в том числе и в нашей стране, проводились в 1920-е и 1930-е гг. Тем не менее, активно использовать этот метод лечения начали только в 1990-е гг., и в последнее десятилетие популярность только растет.
Для чего используется пересадка костного мозга
По словам Ларисы Анатольевны Кузьминой, кандидата медицинских наук, заведующей отделением химиотерапии гемобластозов и трансплантации костного мозга и гемопоэтических стволовых клеток НМИЦ гематологии Минздрава России, одна из причин роста популярности аллогенной (от одного человека к другому) трансплантации костного мозга — это существенное расширение списка болезней, при которых может быть назначена пересадка стволовых клеток.
«Хотя основными показаниями к аллогенной трансплантации когда-то были острые лейкозы и хронический миелоидный лейкоз, сегодня процедура успешно используется при широком спектре заболеваний. Сюда входят различные типы злокачественных лимфом, множественная миелома, апластическая анемия и миелодиспластические синдромы. У детей трансплантация костного мозга и гемопоэтических стволовых клеток становится спасительной процедурой не только при онкологических заболеваниях, но и при врожденных патологиях, таких как первичный иммунодефицит и некоторые метаболические нарушения», — рассказала Л.А. Кузьмина.
Причем есть много заболеваний, при которых стандартная терапия не помогает. Нужна именно трансплантация костного мозга. Это касается, например, острых лейкозов и миелодиспластического синдрома (заболевания, связанного с нехваткой клеток в крови, встречающегося в основном у пожилых людей). Кроме того, в группу высокого риска входят пациенты с онкологией, у которых сохраняется большая вероятность рецидива заболевания даже после курса химиотерапии. В этих случаях пересадку стволовых клеток нужно делать в максимально короткие сроки. И здесь мы подходим к основной проблеме — поиску подходящего донора.
Трудно найти донора
Как отмечает Л.А. Кузьмина, раньше в качестве доноров использовались, как правило, ближайшие родственники пациента. Дело в том, что главное требование к донору — чтобы они с пациентом совпадали по HLA-генотипу. Человеческие лейкоцитарные антигены (англ. Human Leukocyte Antigens, HLA) образуют систему, кодирующую молекулы на поверхности клеток, которые иммунная система использует для того, чтобы распознавать свои и чужеродные клетки. То есть если донор и пациент совпадут по этим антигенам, организм пациента при попадании клеток донора скорее всего не воспримет их как чужеродные. А такое сходство чаще всего бывает у близких родственников, и то далеко не у всех. Можно считать, что больному повезло, если у него есть близнец (брат или сестра). В других случаях никакой гарантии совпадения быть не может.
Тем не менее, сходство HLA-генотипа встречается и у людей, не приходящихся друг другу родственниками. Надо сказать, что именно этот метод HLA-типирования дал возможность использовать неродственные клетки. Поскольку трансплантация костного мозга становится все более востребованной, а количество операций растет, необходимо создать общую базу неродственных доноров. Это обеспечит быстрое нахождение подходящего донора для пациента с определенным генотипом. Для этого в 2022 г. был создан Федеральный регистр доноров костного мозга, управление которым было поручено Федеральному медико-биологическому агентству (ФМБА) России.
«Первоначально базы неродственных доноров создавались в основном на базе медицинских организаций нашей страны: в том числе, Первого Санкт-Петербургского государственного медицинского университета им. ак. И.П. Павлова, Национального медицинского исследовательского центра гематологии Минздрава России, Кировского НИИ гематологии и переливания крови. В дальнейшем для быстрого поиска генетически совместимого донора для каждого пациента появилась потребность в объединении этих данных», — объясняет Л.А. Кузьмина.
В конце августа 2025 г. в Федеральном регистре числилось чуть меньше 348 тыс. типированных доноров — то есть тех, которые уже сдали свои образцы и чей HLA-генотип уже исследован. Именно столько людей сейчас выступают потенциальными донорами костного мозга — в случае, если найдется пациент с похожим генотипом. И этого все еще недостаточно. Как утверждается на сайте Федерального регистра, необходимо не менее 500 тыс. доноров, чтобы у каждого пациента был шанс найти своего. Важно понимать, что если речь идет о неродственных донорах, то найти человека со схожим генотипом очень непросто: шанс такого совпадения составляет примерно 1:10000. Именно поэтому популяризация донорства костного мозга — важнейшая задача для медицины.
Как происходит трансплантация костного мозга
Смысл процедуры заключается в том, чтобы перенести здоровые стволовые клетки из организма донора, которые вытеснят злокачественные клетки пациента. Для примера рассмотрим, как это происходит при острых лейкозах. В здоровом состоянии костный мозг образует гемопоэтические стволовые клетки (ГСК). Их также называют кроветворными клетками, потому что потом они созревают и в результате дифференциации превращаются в клетки крови — эритроциты, лейкоциты и тромбоциты. Эти клетки крайне важны для организма — эритроциты отвечают за доставку кислорода в органы и ткани, тромбоциты останавливают кровотечения и обеспечивают свертываемость, лейкоциты нейтрализуют опасность извне, вырабатывая антитела и разрушая чужеродные белки и бактерии. При острой форме лейкоза кроветворные клетки мутируют и теряют способность к созреванию — таким образом, вместо важных для жизнеобеспечения эритроцитов, лейкоцитов и тромбоцитов в крови скапливаются злокачественные мутировавшие клетки. Если же пересадить из организма донора здоровый костный мозг, то он начнет снова вырабатывать здоровые кроветворные клетки, которые будут созревать и выполнять все необходимые функции.
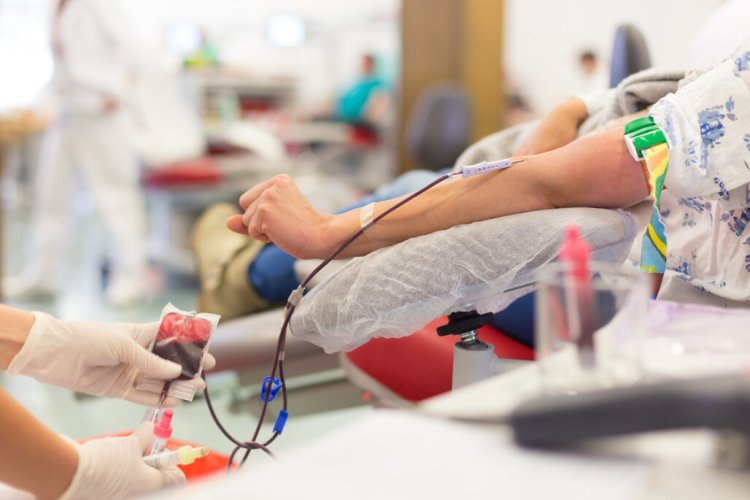
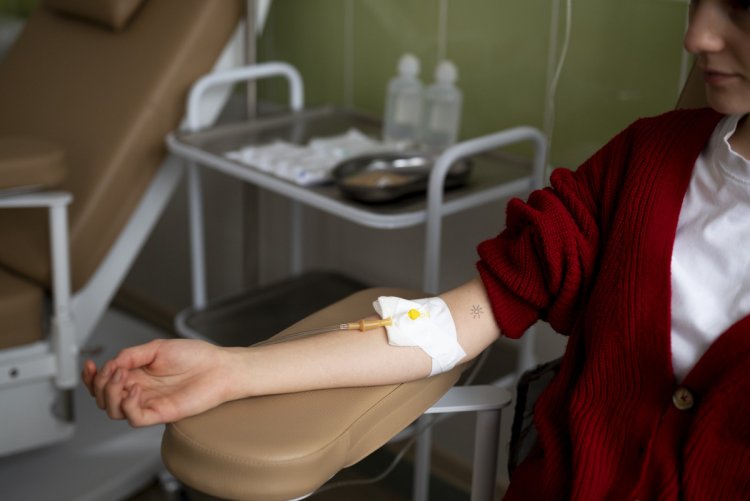
Проблема в том, что неосведомленный человек воспринимает пересадку костного мозга как нечто сложное и пугающее. На самом же деле процедура донации (то есть сдача гемопоэтических стволовых клеток костного мозга для последующей пересадки реципиенту) очень похожа на донорство крови, с той лишь разницей, что перед процедурой донор принимает препарат, который выгоняет стволовые клетки из кости в кровь, и процедура длится три-четыре часа. Препарат может на короткое время вызвать ощущение ломоты в костях и состояние, похожее на симптомы гриппа, но не более того. При этом донор отдает лишь 5% своего костного мозга, и те полностью восстанавливаются в течение семи-десяти дней после процедуры. Их кратковременная потеря никак не сказывается на организме. А вот HLA-типирование ничем не отличается от обычного взятия крови из вены на анализ.
Другой вариант — стволовые клетки берутся напрямую из тазовой кости с помощью шприца. Такая процедура проводится под общей анестезией, и в этом случае пациенту рекомендуют полежать в больнице еще два дня.
Как отмечает Л.А. Кузьмина, именно неосведомленность стала основной причиной того, что доноры отказываются проводить операцию — даже после того, как уже прошли типирование.
«Очень важно активно информировать общество о том, что донорство не имеет ничего общего с травмирующим “извлечением кости”. Современные методы включают в себя сбор стволовых клеток из периферической крови или безболезненный сбор костного мозга под наркозом. Процедура безопасна для донора, и организм восстанавливается», — подчеркнула Л.А. Кузьмина.
Что делать с осложнениями?
Основной проблемой трансплантации костного мозга традиционно считаются возможные осложнения для пациента после процедуры. Особенно это касается последствий иммунологического характера. Но в последнее время медицина смогла серьезно продвинуться в борьбе с ними. Например, одно из наиболее распространенных осложнений при аллогенной трансплантации — реакция «трансплантат против хозяина» (РТПХ). В этом случае клетки донора вступают в конфликт с клетками реципиента, воспринимая их как чужеродные элементы, и при этом страдают внутренние органы — печень и кишечник, а также кожа и слизистые. Острая фаза РТПХ опасна для жизни, но даже если реакция перейдет только в хроническую фазу, она повлечет огромное количество проблем со здоровьем у пациента.
Над этой проблемой ученые работали довольно долго, и сейчас существует несколько путей решения. Это, например, очистка трансплантата, когда с помощью клеточного сепаратора из донорской крови удаляются наиболее «агрессивные» клетки (Т-лимфоциты) — метод, помогающий предотвратить возможную реакцию. Другой вариант — экстракорпоральный фотоферез, когда из крови больного извлекаются лейкоциты и с помощью облучения лишаются своей «чувствительности» — применяется в качестве длительной терапии при хронической РТПХ, когда реакция уже произошла.
Кроме того, в последние годы появился ряд новых препаратов, подавляющих нежелательную иммунную реакцию организма. Например, ученые из НИИ детской онкологии, гематологии и трансплантологии им. Р.М. Горбачевой Первого Санкт-Петербургского государственного медицинского университета (ПСПбГМУ) им. И.П. Павлова в 2022 г. предложили использовать ингибиторы кальциневрина. Они относятся к иммуносупрессорам — средствам, подавляющим иммунный ответ организма. До этого использовались кортикостероиды – гормоны, которые тоже обладают иммуносупрессивным действием, но при этом делают организм пациента более уязвимым перед вирусами и даже рецидивом онкологии. Важное отличие ингибиторов кальциневрина — их более узкий диапазон действия: они не «бьют» по всему иммунитету, а только подавляют активность фермента, из-за которого происходит синтез воспалительных молекул Т-лимфоцитами.
Разумеется, исследования возможностей трансплантации костного мозга и связанных с этим сложностей не прекращаются. Например, долгое время не была достаточно изучена реакция стволовых клеток, которые пересаживают в другой организм. Предполагалось, что пересадка может спровоцировать злокачественные мутации. Однако недавние изыскания американских ученых показали, что такие мутации не связаны с пересадкой. Пересаженные клетки мутировали с такой же частотой, как и те, что остались в организме донора. К тому же эти мутации далеко не всегда приводят к болезням.
Задел на будущее
Сейчас под пересадкой костного мозга подразумевается, как правило, именно трансплантация стволовых клеток. Но костный мозг, помимо кроветворных клеток, содержит еще и строму — соединительную ткань, создающую основу для этих самых клеток. При переливании в кровь донора выгоняются только ГСК, и долгое время считалось, что трансплантация стромальной ткани невозможна.
Летом 2025 г. ученые НМИЦ гематологии совместно с коллегами из Курчатовского института опытным путем смогли доказать, что пересадка стромы возможна — но для этого нужно предварительно ее повредить путем радиационного облучения. Конечно, такой способ предполагает высокие риски. Во-первых, побочные эффекты от высокой дозы радиации. Во-вторых, стромальная ткань донора может и не прижиться в организме пациента — а это уже будет опасно не только для кроветворных клеток, но для всей костной ткани. В общем, как заявил автор исследования Алексей Евгеньевич Бигильдеев, заведующий лабораторией эпигенетической регуляции кроветворения НМИЦ гематологии, перед учеными стоит еще ряд амбициозных задач в этой области. Если их удастся решить, это будет еще одним прорывом, поскольку известно, что при онкологических заболеваниях крови стромальная ткань повреждается как злокачественными клетками, так и химиотерапией.
Источники:
Наука и жизнь. Стволовые клетки крови после пересадки мутируют, как обычно
Правительство Московской области. Почти 4 тыс. человек вступили в федеральный регистр доноров костного мозга в Подмосковье
Национальный медицинский исследовательский центр гематологии. Донорство костного мозга или гемопоэтических стволовых клеток
Федеральный регистр доноров костного мозга
ТАСС. Поврежденный костный мозг оказался более восприимчив к трансплантации
НИЦ «Курчатовский институт». Ученые нашли способ повысить эффективность трансплантации костного мозга
Национальный медицинский исследовательский центр гематологии. Показана принципиальная возможность трансплантации стромы костного мозга
Минздрав России. Что такое HLA-типирование и как оно помогает найти идеального донора костного мозга
Газета.ру. Совместить несовместимое. В технологиях пересадок костного мозга произошла революция
Фото: