Химики из НИУ ВШЭ научились проводить реакцию восстановительного присоединения без внешнего восстановителя. Вместо него «ресурс» дает сам альдегид — один из участников реакции. Это помогает избежать побочных реакций, а также снижает токсичность и упрощает производство и синтез органических молекул — в том числе для производства лекарств. Исследование опубликовано в журнале Journal of Catalysis.
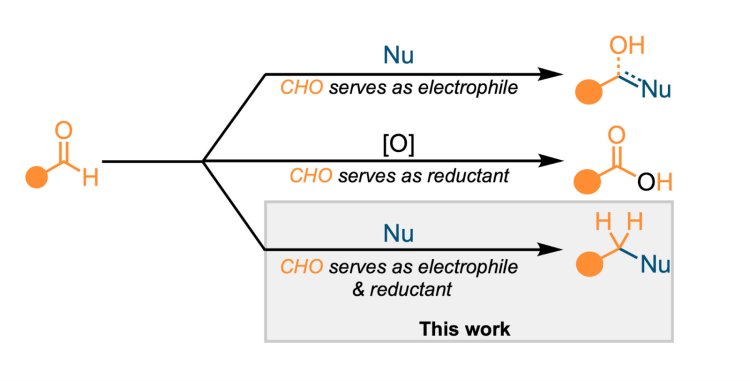
Реакционная активность альдегидов. Альдегиды могут выступать как электрофилы и как восстановители, в этой работе обе роли объединены в одной реакции. © Федор Клюев
Альдегиды — органические молекулы, с которыми человек регулярно сталкивается: с коричным альдегидом и ванилином в выпечке, а с цитронеллалем и цикламеновым альдегидом в парфюмах. При этом многие альдегиды производят миллионами тонн в год, например, н-бутаналь, из которого получают сырье для производства ПВХ, смол и ламинированного стекла. Альдегидная группа встречается и в биологически активных молекулах, например в форме витамина B6 — пиридоксале.
В химическом синтезе альдегиды обычно используют как электрофильные соединения — молекулы, которые принимают электроны и вступают в реакции присоединения. Гораздо реже используют другую их сторону — восстановительную способность, при которой альдегидную группу окисляют, например, до карбоновой кислоты, и молекула отдает электроны.
Исследователи из НИУ ВШЭ и Института элементоорганических соединений им. А.Н. Несмеянова Российской академии наук (ИНЭОС РАН) предложили объединить эти две роли на примере восстановительного алкилирования кетонов — важной реакции, используемой в промышленности, в том числе при синтезе лекарственных соединений. В классическом варианте для такой реакции помимо реагентов требуется внешний восстановитель: водород, борогидриды или монооксид углерода (CO, угарный газ). Это усложняет процесс: восстановители могут быть токсичными или взрывоопасными, вызывать побочные реакции и требовать специального оборудования. В предложенном подходе роль восстановителя берет на себя сам альдегид. Реакция протекает в присутствии рутениевого катализатора и основания, без растворителя и добавления внешнего источника водорода.
«Мы подобрали необходимые условия реакции и предложили концептуально более простую схему: отказаться от дополнительного реагента и использовать альдегид как внутренний источник восстановления. В результате реакцию можно представить не как A + B + С → продукт, а как A + B → продукт, где одна из исходных молекул выполняет двойную функцию», — рассказал Федор Клюев, один из авторов исследования, преподаватель базовой кафедры элементоорганической химии ИНЭОС РАН факультета химии НИУ ВШЭ.
Авторы показали, что метод универсальный: он работает с ароматическими и алифатическими кетонами и альдегидами и при этом сохраняет чувствительные фрагменты молекул — двойные связи и некоторые функциональные группы. Он также подходит и для алифатических альдегидов, хотя обычно в щелочной среде такие соединения реагируют друг с другом и образовывают побочные продукты.
Авторы проверили подход и на других нуклеофилах: аминах, амидах, сульфонамидах и нитрилах — и показали, что его можно использовать не только для построения связей углерод–углерод, но и углерод–азот. Всего в статье приведено около двух десятков примеров, включая синтез противовоспалительного препарата набуметона и производного горомна прегненолона ацетата.
«Мы провели десятки реакций с кетонами, а также проверили, что метод работает и в реакциях с аминами. В дальнейшем мы хотели бы продолжить исследовать уже восстановительное аминирование и доработать наш метод для такого типа реакций. Если нам удастся так же обходиться без внешнего восстановителя в широком наборе случаев, это будет особенно важно для фармсинтеза, где около четверти связей углерод–азот получают именно этим методом», — объяснил Денис Чусов, профессор, заведующий базовой кафедрой элементоорганической химии ИНЭОС РАН факультета химии НИУ ВШЭ.
Исследование выполнено при поддержке гранта РНФ и Минобрнауки РФ.
Информация и иллюстрация предоставлены пресс-службой НИУ ВШЭ