Экспериментатор подносит к своей ладони небольшое устройство, и на экране компьютера появляется детальная сеть больших и малых сосудов, по которым бежит кровь. Это не кадры из фантастического фильма, а съемки из реальной лаборатории: видеть сквозь кожу в реальном времени позволяет сферическая антенна для оптоакустической томографии, созданная учеными из Института прикладной физики им. А.В. Гапонова-Грехова РАН совместно с зарубежными коллегами. Новинка вошла в топ-10 открытий 2025 г. по версии Российского научного фонда, при поддержке которого велась работа над проектом. Одна из потенциальных областей применения инновации — быстрое выявление нарушений в работе сердечно-сосудистой системы и мозга. Как работает и как создавалась уникальная система, названная в научном сообществе «матерью всех антенн»? О настоящем и будущем изобретения корреспонденту «Научной России» рассказывают руководитель проекта, заведующий лабораторией ультразвуковой и оптико-акустической диагностики ИПФ РАН Павел Владимирович Субочев и его коллега, старший научный сотрудник лаборатории биофотоники ИПФ РАН Анна Геннадьевна Орлова.
Музыка света
Оптоакустическая томография построена на способности веществ «звенеть» в ультразвуковом диапазоне в ответ на воздействие лазерных импульсов с правильно подобранными параметрами. Когда материя поглощает частицы света — фотоны, те нагревают среду, в которую попали. В результате плотность вещества меняется, и из-за этого в нем возникают термоупругие сигналы — акустические волны. Этот звук не услышать человеческим ухом, но зато можно поймать с помощью специализированного оборудования.
Каждое вещество или материал по-своему реагирует на фотоны и, как следствие, откликается на облучение разным звуком. Таким образом, по этой «музыке» можно дистанционно определять положение в пространстве различных структур — например, сосудов под кожей.
Оптоакустическая томография позволяет получать и функциональные данные, например о степени оксигенации (насыщения кислородом) крови. Артериальная кровь, богатая кислородом, — ярко-алая, а венозная, уже отдавшая ценный газ организму, — темно-красная. Разный цвет говорит о том, что эти субстанции неодинаково поглощают свет, — соответственно, их акустический отклик на воздействие лазером будет разным. Чтобы оценка оксигенации крови была достаточно точной, для обследования используется быстро сменяющийся свет разного цвета с разной длиной волны.
Руководитель проекта, заведующий лабораторией ультразвуковой и оптико-акустической диагностики ИПФ РАН Павел Владимирович Субочев.
Фото: Ольга Мерзлякова / «Научная Россия»
«Лазер для оптоакустической томографии должен быть импульсным. Это необходимо, чтобы он мог возбуждать в среде звук на разных частотах в широкой полосе, — объясняет кандидат физико-математических наук Павел Владимирович Субочев. — Кроме того, важно, чтобы эти импульсы обладали разными длинами волн (то есть лазер быстро менял цвет излучения), — это позволяет определять степень оксигенации крови».
Возможность неинвазивно рассмотреть сосуды человека и увидеть, какая кровь движется по ним в реальном времени, — актуальная задача, необходимая для раннего выявления и лечения сердечно-сосудистых, нейродегенеративных и онкологических заболеваний. Привычные методы диагностики, такие как УЗИ, КТ и МРТ, не могут обеспечить молекулярный контраст, детализацию и временное разрешение, которые необходимы для решения этой задачи. Другие подходы требуют непосредственного вмешательства в организм. Особые трудности как раз связаны с одновременным наблюдением крупных сосудов и микроскопических капилляров. Что касается оптоакустической томографии, то ее возможности до последнего времени не позволяли полноценно обследовать мельчайшие сосуды в реальном времени — не хватало чувствительности и приемного диапазона.
Впрочем, для сферической антенны, представленной в 2025 г., таких помех уже не существует. Она впервые дает возможность одновременно визуализировать сосуды с очень большой разницей в толщине: диаметром от 3 мм до 30 мкм (что сравнимо с размерами эритроцита). Скорость получения объемных изображений и повышенная детализация технологии помогают увидеть даже микроскопические поры в биологической ткани.
Органная фуга кровеносных сосудов
Полное название нового устройства — многоэлементная широкополосная сферическая антенна на основе пьезополимера. На текущий момент система не имеет аналогов в мире, а ее чувствительность к оптоакустическим сигналам более чем в десять раз выше, чем у устройств из традиционной пьезокерамики.
*Пьезоэлектрические материалы — материалы, способные переводить механическое воздействие в электрический сигнал. Простой пример — зажигалка с пьезоподжигом: нажатие на кнопку запускает электрический импульс, а тот помогает «высечь искру». В случае со сферической антенной электроимпульсы возникают в ответ на толчки звуковых волн.
Разработанная исследователями уникальная антенна для оптоакустической томографии включает 512 чувствительных элементов.
Фото: Максим Прудников / предоставлено П.В. Субочевым
Антенна включает чувствительный элемент в виде тончайшей пьезополимерной пленки, а также усилитель, помогающий согласовать сигнал с пленки с аналоговым цифровым преобразователем. На поверхности пьезополимера сформированы 512 чувствительных элементов, каждый площадью менее 1 мм2: такая плотность «упаковки» продемонстрирована впервые в мире. Данные записываются одновременно со всех элементов, работающих независимо друг от друга. Благодаря этим решениям изобретение дает возможность моментально визуализировать трехмерную структуру сосудов в изучаемом объеме.
«Главная особенность нашей антенны в том, что каждый ее элемент — сверхширокополосный (в оригинальной статье используется понятие “ультраширокополосный”). У стандартной широкополосной антенны полоса чувствительности относительно близка к центральной частоте. В нашем случае полоса чувствительности у элементов антенны двукратно превышает центральную частоту: она начинается примерно от 300 кГц и достигает около 30 МГц. Это очень широкий диапазон, — подчеркивает П.В. Субочев. — Я часто провожу аналогию с органной музыкой: трубы органа разного размера издают звуки на различных частотах — тонкие пищат, а толстые гудят. Так и с кровеносными сосудами. Поэтому важно, чтобы каждый элемент антенны мог одновременно “слышать” сосуды разного размера».
Множество чувствительных элементов — ключ к точной визуализации сосудов.
«Когда во время грозы гремит гром, можно с закрытыми глазами определить на слух примерное направление, откуда исходит звук. Но если бы у нас было не два уха, а, допустим, три, при этом расположенных в различных местах, мы могли бы не только определить, в какой стороне находится источник звука, но и оценить его точные координаты на карте, — приводит пример П.В. Субочев. — В нашу антенну включены 512 “слышащих” элементов, что позволяет с высокими точностью и детализацией обследовать как мелкие (на высоких частотах), так и крупные (на низких частотах) структуры в объеме около 1 см3».
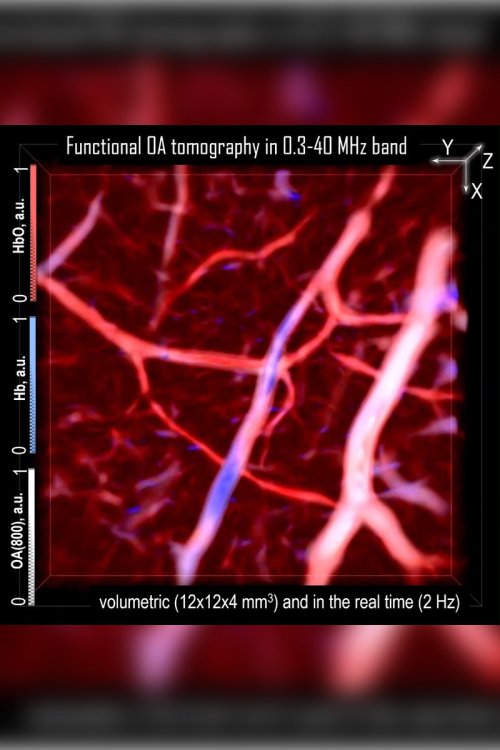
Часть трехмерной карты оксигенации крови в сосудах внутри ладони человека.
Источник изображения: www.photoacoustics.ru / предоставлено П.В. Субочевым (оригинальную видеоверсию можно посмотреть по ссылке)
Прием акустических сигналов на высоких частотах позволяет получать изображение с высокой детализацией. В то же время регистрация низкочастотных волн помогает собирать основные количественные данные и оценивать оксигенацию крови.
Детали разработки исследователи представили в статье в престижном научном журнале Light: Science & Applications с импакт-фактором 23,4 издательства Nature. Путь к публикации занял целых шесть лет: столько времени ушло на рецензирование — проверку работы экспертами. Старания увенчались успехом: более того, изображение антенны украсило обложку выпуска, в котором вышла публикация.
Что скрывается под кожей?
Чтобы испытать антенну, ученые провели несколько экспериментов. Один из них описан в начале этой статьи — визуализация сосудов внутри ладони человека. В другом эксперименте антенна использовалась для неинвазивного обследования головного мозга здоровой мыши. Здесь ученые также ориентировались на оксигенацию: если к участку мозга наблюдается приток богатой кислородом крови, значит в этом месте нейроны работают особенно интенсивно. Такая взаимосвязь называется нейроваскулярным сопряжением.
«С помощью оптоакустической томографии мы не можем непосредственно увидеть нервные клетки, но при нейрональной активности в зоне возбуждения происходит локальное изменение оксигенации. Используя оптоакустическую томографию с воздействием лазера на разных оптических длинах волн, мы можем увидеть, как изменилось содержание окси- и дезоксигемоглобина в крови (гемоглобина, несущего кислород, и уже его отдавшего соответственно. — Примеч. авт.)», — поясняет кандидат биологических наук Анна Геннадьевна Орлова.
В этом испытании у подопытной мыши вызывали сокращение лапки путем электрической стимуляции и отслеживали, как это движение мышц отражалось в работе мозга. Антенна успешно показала включение тех участков, которые действительно отвечают за двигательную активность.
«Проведенные эксперименты — своеобразные примеры для врачей, чтобы они могли познакомиться с нашими возможностями. Если медицинские специалисты посчитают, что нашу разработку можно применить для решения клинических задач, то обратятся к нам для проведения совместной работы. В результате мы сможем собрать доказательную базу эффективности нашего устройства в той или иной области медицины», — поясняет П.В. Субочев.
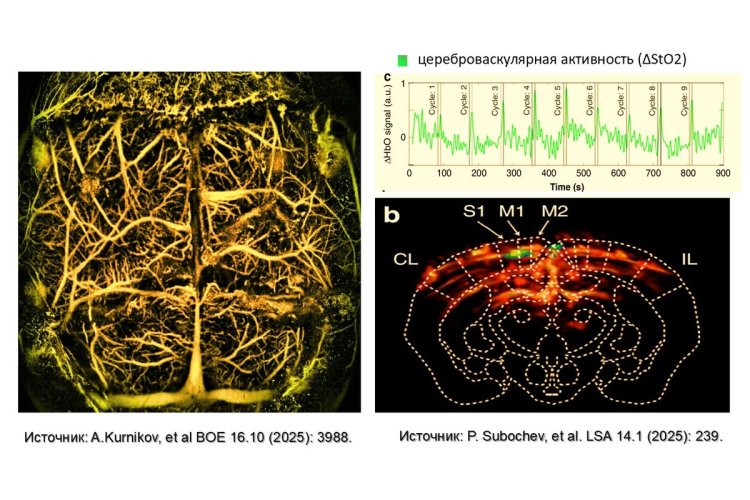
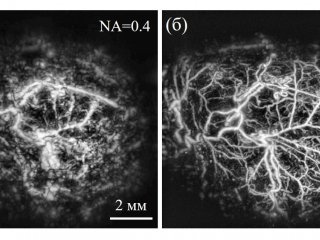
Примеры ангиографических изображений мозга мыши.
Источники изображений: A.Kurnikov, et al. Biomedical Optics Express 16.10 (2025): 3988 (слева); P. Subochev, et al. Light: Science & Applications 14.1 (2025): 239 (справа) / предоставлены П.В. Субочевым
Возможности новой системы можно также оценить по другой статье, опубликованной учеными несколько лет назад совместно с кандидатом медицинских наук, врачом-флебологом Светланой Владимировной Немировой — проректором Приволжского исследовательского медицинского университета (ПИМУ). Эта работа была посвящена испытаниям разработанной коллективом одноэлементной оптоакустической антенны — предшественницы нового изобретения, отличавшейся тем, что она не работала в режиме реального времени. Чтобы получить изображение с ее помощью, нужно было отсканировать нужный участок тела в течение минуты.
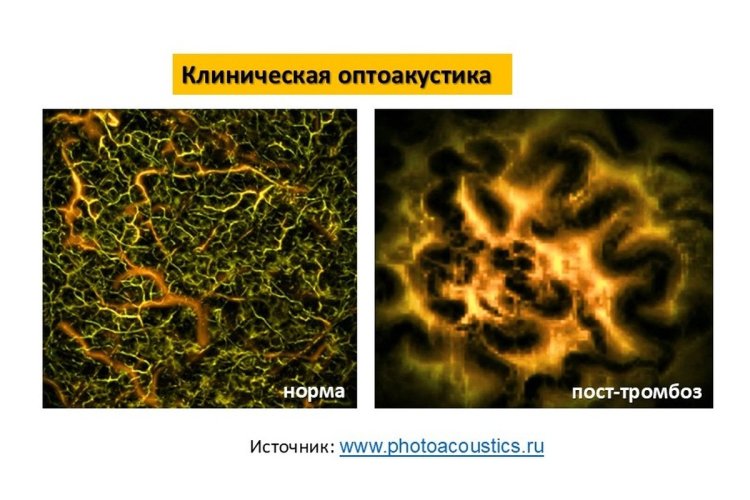
«Нам удалось довольно надежно различать состояние нормы и посттромботический синдром, возникающий в том числе как одно из последствий коронавируса. Тогда вирус еще распространялся активно и эта проблема была особенно актуальной, — вспоминает П.В. Субочев. — Мы обследовали испытуемых во время выполнения функциональных проб: пациенты и здоровые добровольцы либо приподнимали конечность выше уровня сердца, либо опускали ниже, и мы с помощью оптоакустики оценивали состояние их сосудов. В итоге мы доказали, что наша технология может быть полезна при диагностике кровеносной системы».
Клиническая оптоакустическая ангиография (визуализация кровеносных сосудов).
Источник изображений: www.photoacoustics.ru / предоставлены П.В. Субочевым
Нефтяные пленки и дефекты в оптике
Антенне можно найти и применения, не связанные с медициной. Так, исследователи использовали ее для оценки толщины нефтяной пленки на поверхности воды.
«Сырая нефть близка к крови по оптическим свойствам на длине волны 532 нм: в ответ на облучение лазером нефтяные пленки откликаются акустическим сигналом. Мне стало интересно, можно ли с помощью оптоакустики определить толщину нефтяной пленки на поверхности воды, — отмечает П.В. Субочев. — Оказалось, что лазерная оптоакустика действительно на это способна, причем при довольно широком диапазоне толщин. Мы с коллегами-гидрофизиками выпустили публикацию об этом исследовании, но нужно добавить, что пока наша технология испытывалась только в лабораторных условиях».
Руководитель проекта Павел Владимирович Субочев (второй ряд, в центре), старший научный сотрудник лаборатории биофотоники ИПФ РАН Анна Геннадьевна Орлова (крайняя справа) и их коллеги с заместителем председателя правительства Нижегородской области, и.о. министра науки и высшего образования региона Екатериной Сергеевной Солнцевой (первый ряд, в центре).
Фото: пресс-служба ИПФ РАН
Другой возможный пример использования антенны — неразрушающий контроль качества изделий.
«В данном случае технология правильно называется лазерной ультразвуковой микроскопией, хотя воспроизводимый эффект — чисто оптоакустический, — поясняет П.В. Субочев. — В процессе классического ультразвукового исследования зондирующий импульс производится при помощи электричества. Возможности этого подхода ограничены, да и пьезоэлементы для создания сигнала на очень высоких частотах довольно сложно изготавливать. А если ультразвук генерировать при помощи лазера, переводя лазерный импульс за несколько наносекунд в акустический, можно успешно производить зондирующие сигналы с частотами в сотни мегагерц. Мы пробовали применять этот подход для диагностики качества склеивания оптических элементов. Даже если изделия визуально кажутся идеальными, в них могут скрываться дефекты, связанные с нарушениями в прозрачном клеевом слое. Ультразвук позволяет их обнаруживать. Поскольку масштабы таких дефектов очень малы, для их выявления важны высокочастотные зондирующие импульсы, которые как раз можно генерировать с помощью оптоакустических технологий. Принимая обратно ультразвук, мы можем по его рассеянию осуществлять дефектоскопию. В ИПФ РАН существует мощное лазерное направление, и коллеги-оптики предоставили нам для изучения кристаллы, в которых действительно удалось обнаружить дефекты. Результаты этих исследований также были опубликованы».
П.В. Субочев проводит томографическое оптоакустическое сканирование своей ладони в лаборатории.
Источник изображения: www.photoacoustics.ru / предоставлено П.В. Субочевым (оригинальную видеоверсию можно посмотреть по ссылке)
В поисках идеала
Во время работы в распоряжении проектной команды была французская антенна, очень похожая по геометрической конфигурации на спроектированную ими собственную систему, но выполненная из традиционной пьезокерамики. В дальнейшем это позволило максимально точно сравнивать возможности нового изобретения с уже существующим изделием без погрешностей, связанных с разным строением. В опубликованной статье исследователи демонстрируют преимущества своей разработки по качеству приема сигналов на разных частотах и получаемого изображения.
Именно замена пьезокерамики на пьезополимер позволила ученым добиться высокой чувствительности в широкой полосе приема. Как объясняет П.В. Субочев, пьезокерамическая антенна хорошо улавливает ультразвук на центральной частоте за счет резонанса, а вот при регистрации низких частот (что важно, например, при оценке оксигенации крови) в десять и более раз выигрывает новая антенна из пьезополимера. Обратной стороной замены материала стала необходимость дополнить систему усилительным элементом, причем рассчитанным на все 512 каналов. При этом он должен был располагаться как можно ближе к поверхности пьезопленки, то есть быть практически распаянным на ней.
Замена традиционной пьезокерамики на пьезополимер позволила ученым добиться высокой чувствительности антенны в широкой полосе приема.
Фото: пресс-служба ИПФ РАН
«Пьезопленка хороша своей гибкостью, но эту характеристику важно правильно использовать, — говорит П.В. Субочев. — Для решения нашей задачи нам нужно было превратить плоскую пленку в полусферу. Это легко нарушаемый технологический процесс. Если слишком сильно растянуть пленку, она может порваться или потерять поляризацию. К деполяризации приводит и нагрев этого материала от 70 °C, поэтому еще одна сложность заключается в том, что такую пленку нельзя паять. В результате у нас возникла необходимость искать другие способы создания электрических контактов».
В поисках лучшего пьезополимера для антенны П.В. Субочев сотрудничал и консультировался с производителями из разных стран. Команда протестировала британские, французские и американские пленки. В результате масштабных сравнений ученые остановились на американском материале. А один из членов команды П.В. Субочева, аспирант Алексей Курников, опубликовал в журнале Ultrasonics расширенное исследование, посвященное зависимости чувствительности антенны от характеристик пьезопленки.
В планах исследователей — попробовать повысить доступность изобретения для максимально успешной реализации на рынке. Например, рассматривается идея замены полноценных лазеров на лазерные диоды. Есть идеи и по удешевлению акустических компонентов разработки.
Во время экспериментов в лаборатории исследователи обязательно надевают специальные очки для защиты от лазерного излучения.
Фото: пресс-служба ИПФ РАН
Судьбоносные встречи
На пути к открытию Павла Владимировича Субочева поддерживали и вдохновляли многие коллеги, включая известных ученых.
«Отправной точкой, наверное, правильнее всего считать 2002 г. — год моего поступления в лабораторию ультразвуковой и оптико-акустической диагностики ИПФ РАН, — размышляет П.В. Субочев. — Все это время мы с коллегами так или иначе шли к текущему результату. До 2009 г. я работал инженером под руководством Анатолия Дмитриевича Мансфельда, заведующего лабораторией ультразвуковой диагностики отдела радиофизических методов в медицине ИПФ РАН, и жил экспериментом — проводил испытания в области широкополосной регистрации ультразвука. Сейчас отделом руководит Илья Викторович Турчин, мой непосредственный начальник и соавтор публикации, а мне в 2021 г. досталась лаборатория Анатолия Дмитриевича».
В 2007 г. классик мировой биофотоники Валерий Викторович Тучин познакомил П.В. Субочева с Лихуном Ваном (Lihong Wang) — одним из ведущих мировых специалистов в области оптоакустики, автором знакового исследования, показавшего возможность применения импульсного лазерного излучения с разными длинами волн для решения задач биомедицинской оптоакустики. Лихун Ван одобрил исследования П.В. Субочева в области широкополосной регистрации ультразвука, отметив важность выбранного направления.
Семнадцать лет спустя: Павел Владимирович Субочев и Лихун Ван — выдающийся ученый, который, по мнению П.В. Субочева, может стать нобелевским лауреатом за работы по оптоакустике.
Фото: Валерий Викторович Тучин / предоставлены П.В. Субочевым
На первом месте в списке тех, кому коллектив П.В. Субочева выражает благодарность в новой статье, стоит Иван Михайлович Пеливанов, ученик классика оптоакустики, профессора Московского государственного университета Александра Алексеевича Карабутова, автора известного научного труда «Лазерная оптоакустика». И.М. Пеливанов и А.А. Карабутов не раз приезжали в ИПФ РАН и консультировали коллег. «Одна из первых экспериментальных многоэлементных антенн для широкополосной регистрации ультразвука была сделана для нашей команды руками Ивана Михайловича, чтобы продемонстрировать нам перспективность пьезополимерных пленок», — делится П.В. Субочев.
Судьбоносной стала встреча П.В. Субочева с зарубежным исследователем российского происхождения профессором Даниилом Рязанским. Ученые встретились на конференции, где Павел Владимирович представлял одноэлементные антенны для оптоакустических исследований. Даниил Рязанский проявил интерес к разработкам и предложил П.В. Субочеву изготовить антенну, разбитую на 512 независимых элементов. На тот момент вызов казался практически невозможным, но ученые все-таки приняли решение начать сотрудничество и выиграли грант Российского научного фонда на реализацию проекта. В дальнейшем именно Рязанский предоставил коллегам зарубежную площадку и лабораторных животных для испытания новой антенны.
Безусловно, были и непростые моменты. Самым сложным для коллектива стало двухлетнее отсутствие тематических грантов РНФ, из-за которого ресурсы на продолжение работы существенно сократились. Тогда лабораторию П.В. Субочева спасла президентская стипендия, присужденная ключевым аспирантам, участвовавшим в исследовании.
В команде П.В. Субочева — не только ученые с многолетним опытом, но и талантливые аспиранты.
Фото: пресс-служба ИПФ РАН
Микроскоп для мозга и борьба с раком
Полученные результаты — задел для будущих интересных проектов. На пресс-конференции в МИА «Россия сегодня» в декабре 2025 г. П.В. Субочев анонсировал планы по созданию на основе новой антенны мультимодального медицинского микроскопа, способного визуализировать не только кровеносные сосуды, но и нейрональную активность. Исследователи уже выиграли грант РНФ на реализацию разработки совместно с зарубежными партнерами.
В отличие от поставленного ранее эксперимента, где нейрональная активность определялась по оксигенации крови, ученые планируют обратиться к использованию флуоресцентных меток, таких как зеленый флуоресцентный белок GFP (Green Fluorescent Protein). В этой работе важную роль наравне с физиками будут играть химики и биологи.
«Оптоакустические технологии не позволяют видеть нейрональную электрическую активность в чистом виде, поскольку этот метод основан на распознавании оптического контраста, — поясняет А.Г. Орлова. — Но нейрональную активность и оптический контраст все же можно связать в режиме реального времени. Существуют специальные флуоресцентные белки, которые начинают светиться только в момент встречи с ионами кальция — главными маркерами нейрональной активности. Если мы научим нашу антенну “слышать” оптическое поглощение этих белков, мы сможем наблюдать за работой мозга в реальном времени».
Отслеживание ионов кальция дает возможность более оперативно наблюдать за изменением нейрональной активности. В случае с диагностикой по окислению крови задержка составляет около 10 с.
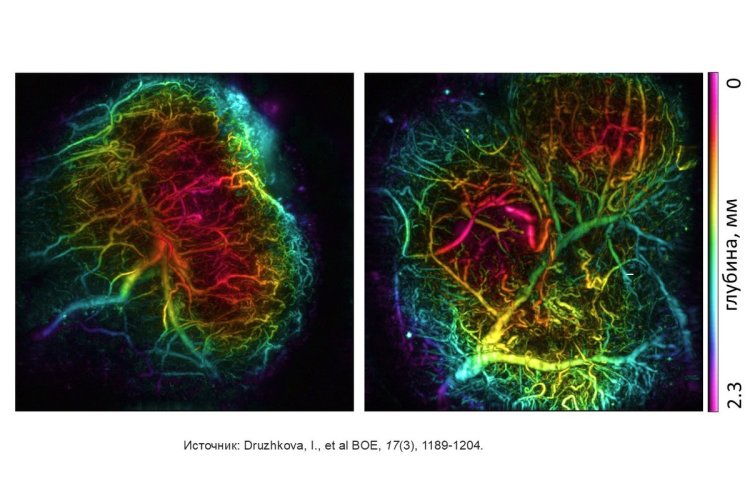
Исследования кандидата биологических наук Анны Геннадьевны Орловой: применение оптоакустики в экспериментальной онкологии.
Источник изображений: Druzhkova, I., et al. Biomedical Optics Express, 17(3), 1189-1204 / предоставлены П.В. Субочевым
«Альтернатива GFP, обсуждаемая учеными, — красные флуоресцентные белки, которые даже выгоднее использовать с точки зрения оптоакустики, поскольку их свечение можно регистрировать на бóльших глубинах, — подхватывает П.В. Субочев. — Обычно для детектирования флуоресцентных белков на большой глубине используются многофотонные флуоресцентные методы. Но эти соединения, не обладая стопроцентным квантовым выходом флуоресценции, тоже способны термализовывать часть поглощенной оптической энергии, поэтому их можно использовать и для оптоакустических исследований. Классический пример — статья нашего коллаборатора Даниила Рязанского, опубликованная в 2009 г. в журнале Nature и продемонстрировавшая возможность визуализации флуоресцентных белков при помощи оптоакустики. Поэтому мы вместе с зарубежными партнерами думаем, что если повысим чувствительность наших антенн, то тоже сможем детектировать такие белки по их оптическому поглощению».
«Таким образом, если мы будем использовать специальные сенсоры, способные указать на работу нейронов (реагирующие на изменение содержания ионов кальция или иной признак), и они будут отличаться определенным оптическим поглощением на каких-либо длинах волн, то их тоже можно будет увидеть», — подытоживает А.Г. Орлова.
Другая задача «со звездочкой», для решения которой исследователи хотят использовать оптоакустическую антенну, — визуализация сторожевых лимфатических узлов при онкологических заболеваниях. Это первые лимфоузлы на пути лимфы, оттекающей от опухоли, и наблюдение за ними важно для борьбы с раком.
«Лимфатическая система не имеет явного оптического контраста, из-за чего недоступна для прямой диагностики с помощью оптоакустики, — сообщает П.В. Субочев. — Поэтому мы планируем тесно сотрудничать с химиками, разрабатывающими специализированные контрастные агенты, которые окрашивают ее при введении в лимфатическую систему. При наличии таких веществ мы сможем повторить протокол более ранних исследований с оценкой оксигенации крови, просто вместо окси- и дезоксигемоглобина установить концентрацию контрастных агентов. Хорошие перспективы в качестве такого агента у индоцианина зеленого (ICG), разрешенного для клинического использования. Но в целом химия, как и любая наука, стремится к прогрессу, и наши коллабораторы из Сколтеха во главе с профессором Дмитрием Александровичем Гориным научились совершенствовать контрастные агенты ICG, упаковывая их в наночастицы и управляя как шириной линии их оптического поглощения, так и абсолютным значением поглощения (молярным коэффициентом экстинкции). Для проверки токсичности новых химических соединений мы планируем сотрудничать с нашими давними коллабораторами-биологами, группой Марины Александровны Сироткиной в ПИМУ».
Работа в «чистой комнате» — беспыльном помещении, где находятся оптические столы с лазерами.
Фото: пресс-служба ИПФ РАН
На передовой науки
Сейчас ученые уже располагают всем необходимым для проведения экспериментов на своей территории. П.В. Субочев подчеркивает, что обрести самостоятельность и оборудовать собственную лабораторию команде во многом помогла грантовая поддержка проекта НЦМУ «Фотоника», выполнявшегося под руководством академика Ефима Аркадьевича Хазанова.
«В нашем распоряжении сейчас есть лаборатория площадью 110 м2, спроектированная нами самими по высокоуровневым зарубежным лекалам. Благодаря поддержке моего непосредственного руководителя Ильи Викторовича Турчина у нас есть и перестраиваемый лазер, и аналого-цифровой преобразователь, и портативная версия антенны: у текущего варианта, который мы используем, количество элементов было решено сократить до 256, — рассказывает Павел Владимирович Субочев. — Наша новая лаборатория включает как инженерное помещение, где можно паять и заниматься аддитивным инжинирингом, при этом отходы выбрасываются наружу в атмосферу, так и “чистую комнату” — беспыльное помещение с приточной вентиляцией, где у нас находятся оптические столы с лазерами. Условия в лаборатории позволяют заниматься как созданием антенн, так и оптоакустическими экспериментами, в том числе совместными с биологическими институтами и клиническими центрами. Например, один из наших партнеров — Российский онкологический научный центр им. Н.Н. Блохина. Таким образом, мы проделали большую работу, и сегодня это очень помогает в нашем дальнейшем развитии».
Источники
Комментарии П.В. Субочева
Комментарии А.Г. Орловой
Выступление П.В. Субочева на пресс-конференции «Топ-10 научных открытий года» в декабре 2025 г., проведенной МИА «Россия сегодня» и Российским научным фондом
Российский научный фонд. Сферическая антенна из пьезополимера позволила наблюдать за кровотоком в реальном времени
Фото на превью: пресс-служба ИПФ РАН.
Источник изображений на главной странице: Druzhkova, I., et al. Biomedical Optics Express, 17(3), 1189-1204 / предоставлены П.В. Субочевым.
Источники изображений в тексте: Ольга Мерзлякова / «Научная Россия», пресс-служба ИПФ РАН, Максим Прудников / предоставлено П.В. Субочевым, www.photoacoustics.ru / предоставлены П.В. Субочевым, A.Kurnikov, et al. Biomedical Optics Express 16.10 (2025): 3988 / предоставлено П.В. Субочевым, P. Subochev, et al. Light: Science & Applications 14.1 (2025): 239 / предоставлено П.В. Субочевым, Валерий Викторович Тучин / предоставлены П.В. Субочевым, Druzhkova, I., et al. Biomedical Optics Express, 17(3), 1189-1204 / предоставлены П.В. Субочевым.