Биосовместимые магнитные наночастицы из оксида железа (маггемита) для лечения раковых опухолей разработала команда ученых из уральских университетов и институтов. Технологии еще предстоит пройти множество испытаний, но в перспективе такие частицы можно будет подсаживать в клетки для последующей управляемой доставки в нужное место организма и уничтожения злокачественного новообразования. Инновация может стать ценным подспорьем в борьбе со всеми видами опухолей, включая плохо поддающиеся химиотерапии, например, меланому и рак прямой кишки.
Цель проекта — усовершенствовать дендритно-клеточную иммунотерапию рака. В ее основе лежит воздействие на собственные (аутогенные) дендритные клетки пациента. Это своеобразные «информаторы», играющие важнейшую роль в запуске иммунного ответа на заболевание за счет того, что «поднимают тревогу» среди клеток-«охранников» — T-лимфоцитов, представляя им антигены1 опухоли. После этого активированные T-лимфоциты, «изучив» противника, получают возможность целенаправленно атаковать раковые клетки.
Дендритно-клеточная иммунотерапия онкозаболеваний проходит следующим образом: врачи берут моноциты2 из крови пациента, получают из них дендритные клетки3, после чего «насыщают» их антигенами раковых клеток и с подкожной инъекцией вводят обратно в организм, где модифицированные дендритные клетки запускают иммунную реакцию. Испытания показали, что этот метод может помогать в борьбе с некоторыми видами рака, однако он не получил широкого распространения из-за низкой эффективности. Дело в том, что из получившейся вакцины только около 5% обработанных дендритных клеток успешно добираются до лимфоузлов, где они должны «познакомить» с антигенами T-лимфоциты.
Улучшить действие этой терапии можно было бы, сделав дендритные клетки управляемыми. Для этого в них и планируется внедрять созданные уральскими учеными наночастицы в составе специальной суспензии. Затем обработанные клетки можно будет с помощью внешнего магнитного поля целенаправленно переместить к лимфоузлам. Наблюдать за распространением наночастиц позволит магнитно-резонансная томография (МРТ).
Ценные особенности полученных наночастиц делают их перспективным медицинским материалом. Об этом корреспонденту «Научной России» рассказала соавтор работы, профессор-исследователь кафедры магнетизма и магнитных наноматериалов Уральского федерального университета, доктор физико-математических наук Галина Владимировна Курляндская.
«Используемые нами наночастицы оксида железа (маггемита) обладают малой цитотоксичностью, — отметила Г.В. Курляндская. — Особенно интересны их магнитные свойства, которые и позволяют предлагать новые методы лечения. Данные частицы суперпарамагнитны, то есть без внешнего магнитного поля у них нет магнитного момента и они не взаимодействуют друг с другом. Это очень важное свойство, так как именно отсутствие магнитного взаимодействия без внешнего поля предотвращает “слипание” частиц внутри живого организма. При этом приложение внешнего магнитного поля приводит к появлению магнитного момента суперпарамагнитных частиц, а значит, ими можно управлять и направлять их в зону терапии. Такие частицы могут играть роль носителей необходимого лекарства для его локального применения, а находясь внутри живой клетки, могут способствовать ее миграции в зону терапии».
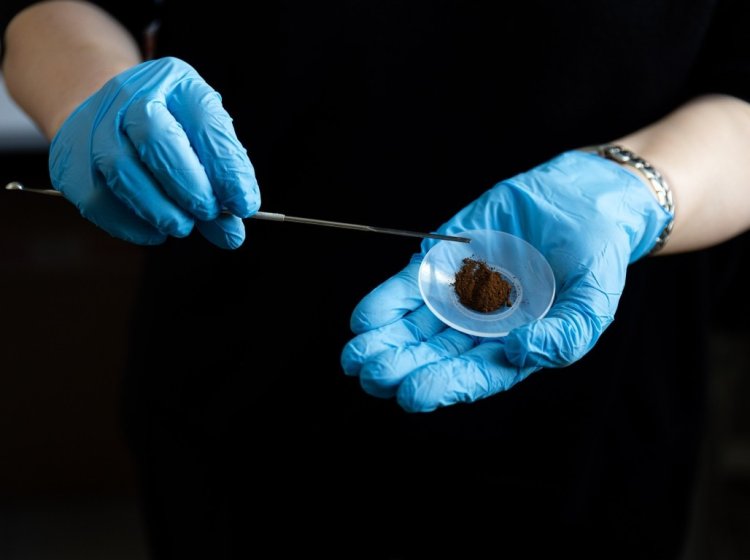
Образец суспензии магнитных наночастиц, который испытывался на живых клетках.
Фото: Родион Нарудинов / УрФУ
Для управления магнитоактивными клетками потребуется специальная магнитная система. У исследователей уже есть опыт успешного решения подобных задач.
«Прежде всего, следует отметить, что специальные устройства, создающие магнитные поля заданной конфигурации, мы разрабатываем и создаем давно. Например, ранее мы исследовали влияние постоянного магнитного поля на скорость пролиферации4 фибробластов человека, выращенных на различных субстратах: полистироле, полиакриламидном гидрогеле и феррогеле, содержащем магнитные наночастицы маггемита. Для решения этой задачи мы создали и аттестовали магнитную матрицу, состоящую из 24 постоянных магнитов. Она успешно использовалась для выращивания клеточных культур. Поскольку коммерческих аналогов данного устройства тогда просто не существовало (да и сейчас они отсутствуют), к нам поступали запросы от различных групп биологов о возможности приобретения данной системы. Одним словом, магнитная система потребуется, но на кафедре магнетизма и магнитных наноматериалов УрФУ решить данную задачу не составит большого труда», — подчеркнула Г.В. Курляндская.
Разработка — результат совместных изысканий УрФУ, Уральского государственного медицинского университета, Института медицинских клеточных технологий Уральского отделения РАН и Института электрофизики УрО РАН.
«Этот виртуальный коллектив сложился около 15 лет назад. У нас часто бывают совместные проекты-гранты, иногда это сотрудничество ведется в рамках государственных заданий. Мы опубликовали более 30 совместных работ в рейтинговых журналах. Главное, что каждый специализированный коллектив решает конкретную подзадачу, а сложенные вместе подзадачи позволяют отвечать на сложные вопросы мультидисциплинарного характера, — пояснила Г.В. Курляндская. — Электрофизики синтезируют наночастицы и аттестуют их физическими методами. Химики исследуют образцы, используя свои подходы, но главное — создают устойчивые водные суспензии, без которых биологические приложения частиц невозможны. Биологи используют магнитные суспензии для экспериментов с клеточными культурами, включая тесты на токсичность. Магнитологи не только аттестуют частицы, суспензии и биоматериалы, содержащие частицы, но и создают магнитные системы и детекторы, способные бесконтактно оценить содержание наночастиц в биообразце. Медики и биофизики формулируют конкретную конечную задачу и предлагают пути ее достижения».
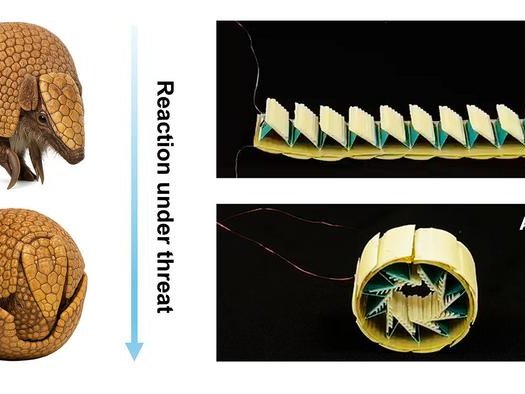
Магнитоактивные клетки планируется перемещать по организму не по одной, а в виде микроскопических сферических конструкций. Исследователям еще предстоит продумать принципы формирования таких клеточных платформ и управления их перемещением с помощью магнитного поля. Деталями этой части проекта с корреспондентом «Научной России» поделился профессор кафедры медицинской физики, информатики и математики УГМУ, профессор кафедры физики конденсированного состояния и наноразмерных систем и кафедры сервиса и оздоровительных технологий УрФУ, доктор биологических наук Феликс Абрамович Бляхман: «В качестве каркаса для трехмерных структур из магнитоактивных дендритных клеток планируется использовать микросферы из биосовместимых гидрогелей. Предполагается, что клетки с частицами будут прикрепляться к поверхности сферы за счет адгезии5, образуя при этом транспортную платформу для управляемой магнитным полем миграции в подкожной клетчатке. Творческий коллектив уже сделал большой задел в части синтеза биосовместимых микросфер размером 100–250 микрометров. Взаимодействие дендритных клеток с микросферами еще предстоит исследовать».
Для экспериментов ученые получили 100 граммов магнитных наночастиц путем электрофизического испарения лазерной мишени. С точки зрения биомедицины это большая партия: такого количества достаточно для множественных испытаний и производства стандартизированных вакцин. Все частицы оказались крошечными сферами с диаметром около 14 нанометров. Это важно, поскольку для того, чтобы создавать качественные водные суспензии для биомедицинских манипуляций, как раз нужны наночастицы с одинаковыми формой и размерами.
Подробнее о разработке корреспонденту «Научной России» рассказали профессор-исследователь кафедры магнетизма и магнитных наноматериалов УрФУ Г.В. Курляндская и профессор УГМУ и УрФУ Ф.А. Бляхман.
Фото: Родион Нарудинов / УрФУ
Исследователи уже изучили физико-химические и магнитные свойства полученных частиц, разработали для них подходящую суспензию, а также оценили успешность внедрения наночастиц в клетки и их токсичность для организма.
Эксперименты показали, что наночастицы могут либо проникать внутрь клеток, либо прочно прикрепляться к их поверхности. Разницы между этими вариантами нет: это не влияет на взаимодействие частиц с внешним магнитным полем. Эффективность перемещения магнитоактивных дендритных клеток определяют два других показателя: количество наночастиц в одной клетке и магнитные свойства каждой такой частицы по отдельности.
Ученые заключили, что наночастицы токсичны для клеток лишь в высоких концентрациях, а вот в небольших количествах, наоборот, повышают их выживаемость и биохимическую активность.
«С биологической точки зрения, частицы обладают малой токсичностью. Мы многократно подтвердили это в ходе предварительных экспериментов на различных типах клеток, среди которых — фибробласты, хондроциты и стволовые клетки. Кроме того, наночастицы в составе синтетических имплантатов на основе гидрогелей не вызывали выраженной реакции иммунного отторжения. Данный факт имеет принципиально важное значение с точки зрения биосовместимости материалов, используемых в контексте разрабатываемой технологии», — подчеркнул Ф.А. Бляхман.
В процессе работы исследователям все время приходится соблюдать особый баланс. С одной стороны, наночастицы не могут быть слишком маленькими, поскольку с уменьшением диаметра ухудшаются и их магнитные свойства. С другой стороны, неправильно подобранные размер и форма частиц, как и неподходящий способ стабилизации суспензии плохо влияют на состояние клеток. Таким образом, ученые стремятся найти равновесие между требуемыми магнитными характеристиками частиц и приемлемым откликом клеток на их внедрение.
Исследователи полагают, что разработанная ими технология может лечь в основу перспективной магнитоуправляемой иммунотерапии. В ближайшем будущем они планируют продолжить изыскания и провести эксперименты по влиянию внешнего магнитного поля на мобильность магнитоактивных дендритных клеток.
Работа получила поддержку Российского научного фонда (проект № 25-24-00175). Результаты исследования опубликованы в журнале Materials.
1Антиген — вещество, определяемое организмом как чужеродное и вызывающее иммунный ответ, направленный на удаление этого соединения. Как правило, антигены выделяют попадающие в организм возбудители заболеваний или опухолевые клетки.
2Моноциты — разновидность белых кровяных клеток — лейкоцитов. Длительность их существования в кровотоке — от 1,5 до 3 суток. После этого они мигрируют в ткани и превращаются в макрофаги (клетки иммунной системы, активно перемещающиеся и «поедающие» чужеродные молекулы, микроорганизмы и клетки, а также погибшие собственные клетки организма) и дендритные клетки.
3Дендритные клетки — клетки, участвующие в запуске иммунного ответа. Они перерабатывают чужеродные антигены и передают их для распознавания одному из видов T-лимфоцитов — клеткам иммунной системы, непосредственно отвечающим за борьбу с болезнью.
4Пролиферация — образование новых клеток путем митоза (деления, при котором обе дочерние клетки получают тот же генетический материал, что и клетка-«родитель»). Лежит в основе роста и дифференцировки тканей.
5Адгезия (от лат. «прилипание, притяжение») — простыми словами, слипание, сцепление поверхностей разнородных материалов (жидкостей или твердых тел) при контакте.
Источник определений: Большая российская энциклопедия (электронная версия). Использованы статьи: «Антиген» (А.А. Ярилин), «Моноциты» (А.А. Ярилин), «Иммунная система» (А.А. Ярилин), «Пролиферация», «Адгезия» (А.Д. Зимон).
Новость подготовлена при поддержке Министерства науки и высшего образования РФ
Фото на превью и на странице: Родион Нарудинов / УрФУ