Ингибируя определенное семейство ферментов, можно разработать новые методы лечения нейродегенеративных заболеваний от глаукомы до болезни Альцгеймера, - пишет eurekalert.org со ссылкой на PNAS.
Многие нейродегенеративные состояния, от глаукомы до болезни Альцгеймера, характеризуются повреждением аксонов - длинных тонких выступов, которые проводят электрические импульсы от одной нервной клетки к другой, облегчая клеточную связь. Повреждение аксонов часто приводит к поражению нейронов и гибели клеток.
Исследователи знают, что ингибирование фермента, называемого двойной киназой лейциновой молнии (DLK), по-видимому, надежно защищает нейроны в широком диапазоне моделей нейродегенеративных заболеваний, но DLK также подавляет регенерацию аксонов. До сих пор не существовало эффективных методов модификации генов для улучшения долговременного выживания нейронов и ускорения регенерации.
Группа из нескольких университетов во главе с исследователями из Медицинской школы Сан-Диего Калифорнийского университета и Института зрения Шили при Калифорнийском университете в Сан-Диего определила еще одно семейство ферментов, называемых киназой четырех зародышевых клеток (GCK-IV киназа), ингибирование которых является сильным нейропротектором, а также разрешает регенерацию аксонов, что делает его привлекательным терапевтическим подходом для лечения некоторых нейродегенеративных заболеваний.
«Мы в основном выяснили, что существует набор генов, которые при ингибировании позволяют клеткам зрительного нерва выживать и регенерировать, - сказал старший автор Дерек Велсби - доктор медицинских наук, доцент офтальмологии в семейном отделении офтальмологии Институте офтальмологии в Шили. - До этой работы ученые знали, как заставить эти клетки выжить, но не регенерировать. И наоборот, есть способы стимулировать регенерацию, но тогда выживаемость была довольно скромной. Конечно, для успешной стратегии восстановления зрения нам нужно и то, и другое, и это шаг в нужном направлении».
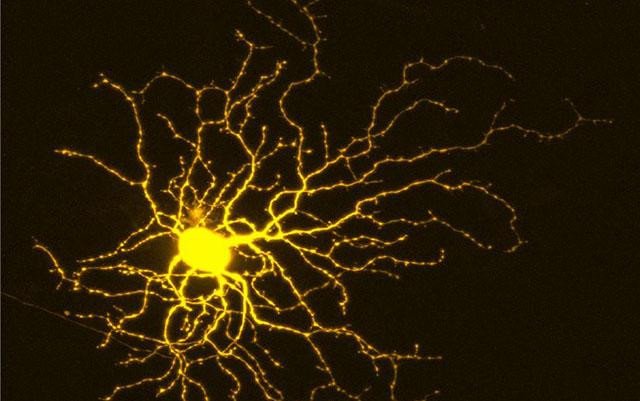
Исследователи провели серию скринингов после создания ганглиозных клеток сетчатки (RGC) из стволовых клеток человека. RGC - это тип нейрона, расположенный около внутренней поверхности сетчатки глаза. Они получают визуальную информацию от фоторецепторов и все вместе помогают передавать эту информацию в мозг.
Первый скрининг включал тестирование группы хорошо изученных химических веществ для оценки их способности увеличивать выживаемость RGC; второй - для измерения способности химикатов способствовать регенерации.
«Затем мы использовали метод машинного обучения, чтобы понять, почему одни соединения активны, а другие - нет, и идентифицировали эти ключевые гены», - сказал Велсби.
По его словам, открытие того, что эти гены улучшают выживаемость RGC, неудивительно. «Однако вы могли бы предположить, что они (как и DLK) будут блокировать регенерацию, когда она запрещена, а не способствовать регенерации. Это определенно было сюрпризом. Это подчеркивает одно из преимуществ науки, основанной на открытиях, с использованием высокопроизводительного скрининга: путем тестирования многих агентов сразу, мы можем идентифицировать пропущенные гены, которые, возможно, не играли роли».
Велсби и его коллеги сосредоточили свою работу на RGC, потому что их интересуют оптические невропатии, такие как глаукома. «Большинство людей думают о глаукоме только с точки зрения «глазного давления», - сказал Уэлсби. Но глазное давление - это только часть проблемы. По своей сути, глаукома представляет собой нейродегенеративное заболевание, характеризующееся прогрессирующей потерей RGC и их аксонов, что приводит к измеримым структурным и функциональным повреждениям зрительного нерва, нарушению зрения и слепоте.
Центры США по контролю и профилактике заболеваний оценивают, что 3 миллиона американцев страдают глаукомой. Это вторая ведущая причина слепоты во всем мире.
Велсби предупредил, что пока не известно, распространяются ли эти
открытия на другие типы нейронов, но он отметил, что эта работа
предполагает сильные терапевтические возможности.
[Фото: eurekalert.org]