Российские ученые с помощью компьютерного моделирования обнаружили, что избыточное количество цинка замедляет развитие болезни Альцгеймера. Этот металл включается в состав скоплений нейротоксичных белков, которые образуются в мозге во время заболевания, поэтому ранее считалось, что он только способствует их появлению. Открытие поможет разработать новые способы борьбы с нейродегенеративными заболеваниями на ранних стадиях. Результаты исследования, поддержанного грантом Российского научного фонда (РНФ), опубликованы в журнале International Journal of Molecular Sciences.
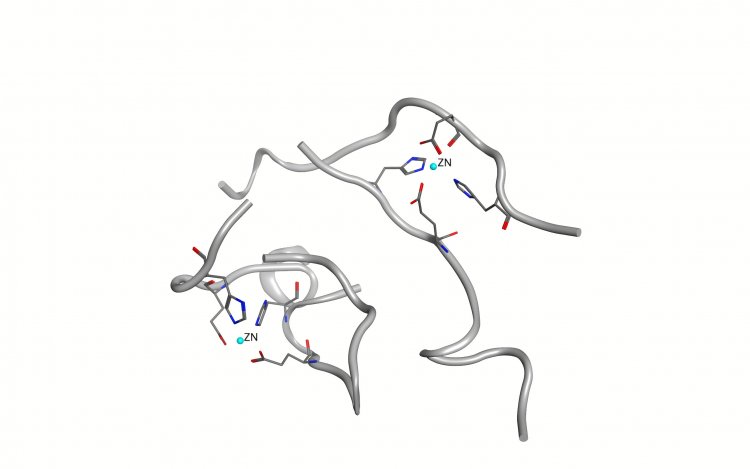
Модель начальной стадии образования агрегатов из амилоидов, в которой четыре белковых молекулы соединяются с двумя ионами цинка. Источник: Алексей Аджубей
Развитие у пожилых людей нейродегенеративных заболеваний — одна из серьезнейших проблем современной медицины, особенно с учетом тенденции к старению населения Земли. Многие из расстройств, в том числе болезнь Альцгеймера, пока не поддаются лечению, и, чтобы разработать лекарственные препараты, крайне важно понимать причины появления патологий.
На молекулярном уровне развитие болезни Альцгеймера вызывают амилоиды — неправильно свернутые белки. Они не только повреждают клетку, в которой образуются, но и «портят» другие белки, запуская сложный цепной процесс, приводящий к появлению нейротоксичных скоплений — амилоидных бляшек. Такие структуры закупоривают сосуды мозга и становятся одной из причин гибели нейронов. Исследования структуры амилоидов показали, что в них содержатся ионы двухвалентных металлов, в частности цинка. Они помогают создавать связи между отдельными молекулами неправильно свернутых белков, что ускоряет образование нейротоксичных агрегатов.
В своей новой работе химики из Института молекулярной биологии имени В.А. Энгельгардта РАН (Москва) создали компьютерную модель, воспроизводящую взаимодействие ионов цинка с молекулами амилоидов, и выяснили, что роль этого металла не так очевидна, как полагали ранее. Химики смоделировали три случая: когда количество ионов цинка не превышало число молекул амилоидов, когда металл находился в избытке и когда его совсем не было.
Оказалось, что, если цинка было в несколько раз меньше, чем молекул амилоидов, нейротоксичные агрегаты образовывались очень быстро. Когда ионы металла присутствовали в избытке, реакция практически полностью прекращалась. Это происходило благодаря тому, что цинк присоединялся ко всем особым участкам амилоидов (координационным центрам), которые могли бы связаться с соседними белковыми молекулами в процессе образования агрегатов. Принцип таков, что ион может взаимодействовать с центрами нескольких белков сразу, служа мостиком между ними. Однако если цинка слишком много, он займет все доступные «посадочные места», молекулам не придется делить один ион, а значит, связи между ними тоже не образуется. Таким образом, ионы металла разрывали цепочку патологичных взаимодействий.
«Наша работа показала, что роль цинка в развитии болезни Альцгеймера противоречива. Исследование поможет в будущем разработать лекарства нового типа для борьбы с ней. В дальнейшем мы планируем изучить роль других металлов, входящих в состав амилоидов, в процессе образования нейротоксичных агрегатов», — рассказывает Алексей Аджубей, кандидат физико-математических наук, ведущий научный сотрудник Института молекулярной биологии имени В.А. Энгельгардта РАН.
Информация и фото предоставлены пресс-службой Российского научного фонда