«Спутник V» стал первой в мире зарегистрированной вакциной от коронавируса и уже спас миллионы жизней. Однако процесс разработки и внедрения этой вакцины сопровождался таким количеством споров и дискуссий, что мы решили обратиться к ее создателю напрямую. Директор старейшего в нашей стране Национального исследовательского центра эпидемиологии и микробиологии им. Н.Ф. Гамалеи Александр Леонидович Гинцбург не боится острых и неудобных вопросов, не прячется и не скрывает проблем, но свято верит в дело, которым занимается.
Александр Леонидович, сегодня все знают о вакцине «Спутник V», спасшей многие жизни. Но не все знают, что ее появлению предшествовал многолетний период испытаний вакцин на основе аденовирусов. Как все это началось?
Вы совершенно правы. Коллектив нашего института под руководством Б.С. Народицкого в течение последних 25 лет разрабатывал технологию доставки различных генов в организм человека с помощью аденовирусных векторов. Исходно эта технология разрабатывалась не для создания вакцинных препаратов, а для генной терапии, но в силу экономических и других причин на тот момент это оказалось не очень перспективным.
Когда в 2014 г. в Африке разразилась эпидемия вируса Эбола с угрозой выхода на другие континенты. Россия подключилась к решению этой проблемы. Состоялась историческая встреча В.В. Путина с главой ВОЗ Маргарет Чан. где российская сторона взяла на себя обязательство помочь в быстром и оперативном создании вакцины против этой смертельной инфекции.
У нас не было на это нескольких лет, было некогда заниматься ослаблением исходного вирулентного штамма, и мы решили использовать принципиально новую технологию, основанную на аденовирусах, хотя сама технология и такого рода конструкции у нас уже были разработаны. Нам удалось создать за 15 месяцев эффективный и безопасный вакцинный препарат, который прошел все клинические испытания и в течение двух лет успешно использовался в Африке, не допустив распространения эпидемии по миру.
Когда началась пандемия новой коронавирусной инфекции, практически сразу зашла речь о создании вакцины, работающей на тех же принципах. Дело в том, что возбудители COVID19 и Эболы — это РНК-содержащие вирусы, которые очень похожи по своему строению друг на друга, оба используют для проникновения в наши эукариотические клетки специальные молекулярные машины. Сделав ставку на ту же технологию, мы не прогадали. За пять месяцев от получения госзадания до начала клинических испытаний нам удалось пройти весь необходимый путь создания вакцины, которая сейчас получила название «Спутник V».
Кстати, почему такое название?
Я могу ответить на этот вопрос, хотя он не ко мне, а скорее к К.А. Дмитриеву, главе Российского фонда прямых инвестиций. Когда этот фонд начал работать над коммерциализацией и выводом нашего препарата на международную арену, необходимо было присвоить ему хорошее громкое имя. «Спутник»— это чисто русское слово, я бы сказал, родное для нас. Напомним тем, кто в это время еще не жил, что оно возникло в 1957 г. благодаря запуску на околоземную орбиту первого советского искусственного спутника. Это слово полностью ассоциируется с Россией и на всех языках звучит одинаково, что имеет маркетинговое значение. Этот расчет полностью оправдался.
А что значит буква V?
Наверное, для иностранного потребителя это означает Victoria, «победа», что тоже хорошо.
Насколько мне известно, аденовирусы совершенно безопасны для человеческого организма. Однако бытуют страшные легенды, что это болезнетворные микроорганизмы, которые разрушают нас изнутри, н сама вакцина встраивается в геном, делая нас мутантами. Расскажите, почему это невозможно.
С аденовирусами человечество родилось и живет всю историю своего существования, а нам они достались от наших предков — приматов. За это время человечество успело размножиться до 7,5 млрд, то есть на его фертильность аденовирусы никак не повлияли. Они не были замечены ни в онкогенности, ни в мутагенности.
А если говорить конкретно о нашей вакцине, то аденовирусные векторы, которые там используются, созданы таким образом, что генно - инженерным способом у них удалены все гены, ответственные за их размножение. Они неспособны размножаться в нашем организме. Если в результате укола в наш организм вводится 1011 частиц, созданных на основе этих векторов, то плюс к этому количеству одна частица в нашем организме не образуется.
Если так, то никаких возможностей его влияния на наш геном в принципе не может быть. Таким образом, мутации полностью исключены. Неоднократные опыты, проводимые в рамках доклинических и постклинических исследований, по возможности влияния этих векторов на фертильность и потомство показали, что такое влияние отсутствует. Через плаценту векторы не проникают. Хотя вакцина и создана на основе живых вирусов, конечный продукт не представляет собой живой объект, способный к размножению.
А вообще вирус — живой объект? На этот счет существуют разные точки зрения даже в профессиональной среде.
Конечно, вирус — живой объект по той простой причине, что стратегия его существования направлена на размножение. Другое дело, что он не может размножаться вне живого организма, и это его особенность. Размножаясь, он мутирует и в результате мутаций ведет себя по Дарвину — эволюционирует. То, что происходит сейчас в плане вакцинации, показывает нам всю остроту этих проблем. Появляются новые, опасные вариации вируса, и мы должны понимать, как противостоять их натиску, какие вырабатывать новые стратегии для успешной борьбы с COVID-19.
Как вы сказали, главное свойство вирусов — способность к мутациям, в результате которых сейчас появился новый дельта-штамм, оказавшийся более опасным, чем все предыдущие. Вы проводите научные исследования мутаций вирусов. Что здесь удалось важного выяснить?
Да, мы действительно проводим эти исследования, не только потому, что это интересно с точки зрения эволюции вирусов, но и потому что это имеет громадное практическое значение. В последние три месяца дельта-штамм вытеснил все предыдущие варианты COVID-19 и сейчас составляет практически 100% тех штаммов, которые у нас циркулируют.
Как у него это получилось?
Секвенирование, то есть определение нуклеотидной последовательности этого вируса, показывает, что в его последовательности возник ряд точковых замен. Аналогичные замены возникали и у предшествующих штаммов, но здесь обнаружилось интересное свойство: эти точковые замены влияют не только на антигенную специфичность вируса, но и на характер его взаимодействия с нашими клетками.
Если так называемый классический штамм, который впервые появился в Ухане, и все последующие штаммы были антигенно видоизмененными, но попадая в наши клетки, разрывали их и выходили наружу, то данный штамм ведет себя иначе. Он не разрывает в результате размножения эукариотическую клетку, а делает отверстие в мембране соседней клетки и проникает внутрь, не повреждая предыдущую.
Если провести аналогию с многоквартирным домом, он ведет себя как жулик, который проникает в квартиру, но не выходит на лестничную площадку, представляющую собой сосуд, где плавают антитела против него или, иначе говоря, стоит полицейский с наручниками, готовый его арестовать. Он проламывает дырку в стене к соседям и пробирается к ним через нее.
Такая стратегия эффективнее с точки зрения вируса?
С точки зрения защиты от нашей иммунной системы это более успешная стратегия, потому что, находясь все время внутри клетки, он защищен от тех антител, которые могут наработать клетки памяти. Он образует так называемые синцитии, многоядерные крупные клетки, внутри которых он передвигается, формируя необычные патологические структуры. Таким образом, он может размножаться довольно долго, поражая десятки клеток, пока этот мешок покрытых общей мембраной нежизнеспособных клеток механически не лопнет, и тогда огромное количество болезнетворных вирусов вывалится в нашу кроветворную систему.
Концентрация вируса при этом повышается не постепенно, а разом, одностадийно. Иммунная система не успевает наработать антител против такого количества вирусов, и вирус успевает проникнуть в легкие, очень быстро переводя болезнь в тяжелую стадию. Это наблюдают клиницисты. Если раньше у больных все штаммы в течение двух недель или дольше проходили путь от легкой стадии до тяжелой и врачи успевали провести все необходимые лечебные процедуры, а иммунная система успевала наработать необходимое количество антител и нейтрализовать вирус, то сейчас благодаря такой хитрости дельта-штамм проходит тот же путь за четыре-пять дней. Успеть стало значительно труднее.
Что в этой ситуации делать?
Закономерный вопрос. Здесь Минздрав сработал на опережение, и если бы все его послушались, то количество тяжелых и тем более смертельных случаев было бы значительно меньше. Первое — это обязательно вакцинироваться, а второе — для тех, кто вакцинировался, через полгода воспользоваться вариантом «Спутник Лайт». То же самое для тех, кто переболел. Это необходимо сделать для нейтрализации вируса на входе в наш организм, не надеясь на то, что у нас успеют сработать клетки памяти. Надо постоянно поддерживать уровень протективных антител против дельта-штамма, и для этого предназначен первый компонент вакцины «Спутник Лайт».
Можно ли предсказать, какие мутации вируса ожидают нас в будущем, или приходится действовать постфактум?
Математических моделей, которые позволяют прогнозировать в данном случае ход эволюции вируса, не существует. Однако известно, что необходимо иметь современный высокотехнологичный мониторинг штаммов, которые сейчас циркулируют, чтобы, не дожидаясь, когда этот возбудитель займет решающее место в инфекционном процессе, заранее определить его патогенные свойства, вирулентность и способность образовывать необычные структуры — синцитии. Далее необходимо вести жесткий мониторинг этого штамма и разрабатывать все профилактические, диагностические и иммунобиологические подходы для его нейтрализации.
Знаю, что вы работаете над созданием новых, более эффективных вакцин. Чего ожидать здесь? Появится ли универсальная вакцина, способная нейтрализовать любой штамм?
Я бы выделил работы, которые особенно актуальны в течение ближайшего времени. Речь идет о возможности создания вирусоподобных частиц, которые состоят из антигенов различных вирусов. Мы уже сейчас видим, что нас окружают несколько различных антигенных вариантов возбудителей COVID-19, а значит, можно технологически собрать вирусоподобную частицу, которая будет состоять не из одного антигена, а из четырех-пяти вариантов.
С другой стороны, эта частица может состоять не только из антигенов COVID-19, но и из антигенов вариантов вируса гриппа. Наша платформа, которая уже очень хорошо проработана (этим вопросом у нас занимается член-корреспондент РАН Т.В. Гребенникова), выходит на стадию поздней доклиники, а с начала следующего года, мы надеемся, конкретные вакцинные препараты перейдут в стадию клинических испытаний. Это будет действительно универсальная вакцина в клиническом понимании слова.
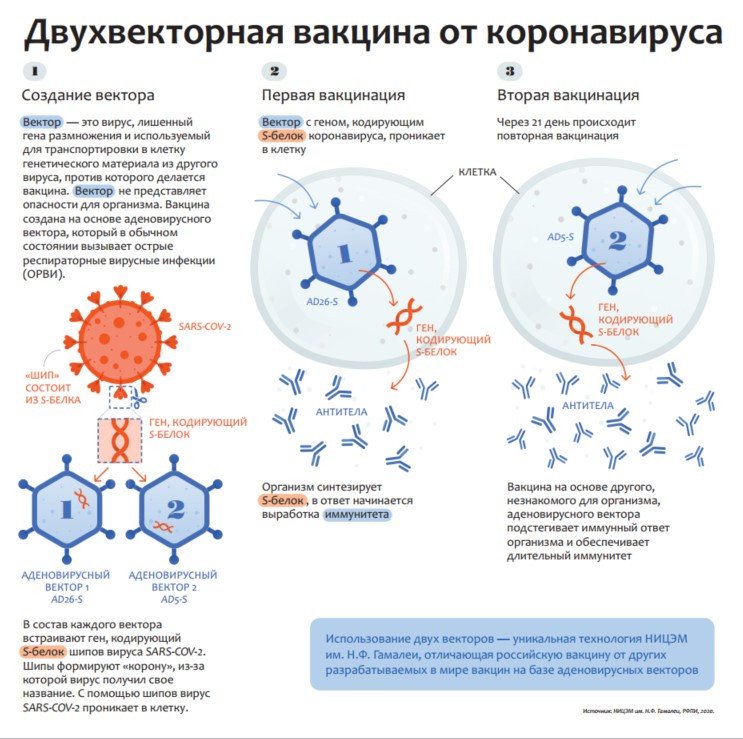
Двухвекторная вакцина от коронавируса
В последние годы человечество стало забывать о роли вирусов в нашей жизни. Много внимания уделялось онкологии, сердечно - сосудистым заболеваниям, разрабатывались новые методы лечения инсультов, что, безусловно, прекрасно, но инфекции как будто ушли на второй план. Пандемия поставила нас на место, напомнив, что никуда от нас такие болезни не денутся. Как вы себе представляете будущее вакцинологии? Появятся ли принципиально новые быстрые вакцины, сверхэффективные и сверхбезопасные, которые избавят человечество от смертельных болезней?
Безусловно, такие исследования будут востребованы, поскольку руководства стран не могут допустить повторения того, что мы переживаем сейчас. Это страшный удар по народонаселению и мировой экономике, поэтому научный потенциал будет направлен на создание универсальных технологий. Об этом не раз говорил и наш президент. Страна должна располагать технологиями, которые будут позволять в течение нескольких месяцев создавать новые вакцинные препараты.
Для этого надо иметь технологические возможности, которые будут быстро реализовываться в зависимости от того, какой возбудитель появится, в создании как новых иммунобиологических, так и терапевтических препаратов, в частности на основе моноклональных антител. Эта технология у нас тоже хорошо разработана и высокоэффективна, хотя стоимость таких препаратов лимитирует их поголовное применение. При этом мы понимаем: если они работают и помогают людям, вопрос цены должен так или иначе решаться.
Мы должны постоянно располагать производственными мощностями, позволяющими в критический момент снабдить население необходимыми препаратами. Сегодня это проблема из проблем, и здесь нужна смелая и мудрая позиция государства — как обеспечить эти мощности в межэпидемический период. Надо иметь очень четкий план с возможностью быстрейшего введения этих как лечебных, так и производственных ресурсов в эксплуатацию, если потребует жизнь. Надеюсь, нынешняя пандемия нас всех этому научила.
Александр Леонидович, как получилось, что вашей профессиональной областью стала именно вирусология?
В 1969 г. я поступил на биофак МГУ и практически сразу выбрал кафедру вирусологии, о чем никогда не пожалел. Академик А.Н. Белозерский,
один из основоположников молекулярной биологии в СССР, который создал эту кафедру, собрал наиболее сильный профессорско-преподавательский состав, что очень привлекало тех, кто хотел посвятить себя научным исследованиям. Я не был исключением. Вирусолог и генетик член - корреспондент РАН В.И. Агол, которому сейчас больше 90 лет, но он по сей день трудится в МГУ, во многом способствовал тому, что я пришел на эту кафедру, а потом он же меня направил на стажировку в иммунологический отдел Курчатовского института, где я получил большой научный опыт. С благодарностью вспоминаю непростые, но очень плодотворные семь лет, когда я писал там свою кандидатскую диссертацию. Все это помогает мне до сих пор, в том числе вот уже 24 года руководить этим институтом.
Ваш институт славен своими научными школами. Как удается их сохранять?
У нас в НИЦЭМ им. Н.Ф. Гамалеи замечательный коллектив. Он сейчас состоит из сотрудников трех больших подразделений. Это сам НИИ эпидемиологии и микробиологии им. Н.Ф. Гамалеи, который всю жизнь занимается болезнетворными микроорганизмами, Институт вирусологии им. Д.И. Ивановского, исследующий патогенные вирусы, и наше производство, делающее, в том числе разнообразные вакцины. Это, например, знаменитая вакцина БЦЖ против туберкулеза, которую получают младенцы в роддомах Москвы, а также многие другие диагностические и лечебные препараты. Теперь это и «Спутник».
Мы гордимся своими научными школами. Б.С. Народицкий, которого я уже упоминал, воспитал множество замечательных учеников. Это, например. Д.Ю. Логунов, которого мы выдвигаем в академики, один из основных разработчиков «Спутника», лауреат Государственной премии нынешнего года. Это И.В. Должикова, Д.В. Щербляков. В. А. Гущин и многие другие.
Очень важны школы В.М. Жданова, Д.К. Львова. Т.В. Гребенниковой. Многие из наших корифеев здравствуют и по сей день работают в нашем институте. У нас трудятся представители одновременно четырех поколений ученых — от 25-летних до 90-летних. Информация внутри школы передается не только с помощью электронных носителей и книг, но и из уст в уста.
Если кому-то необходимо познакомиться с актуальными вопросами менингококковой инфекции, ему не надо рыться в интернете или идти в библиотеку, а можно подойти к Н.Н. Костюковой. Ей 95 лет, но она в течение 15 минут расскажет всю историю вопроса, включая последние молекулярно-генетические инновации, связанные с разработкой диагностических и профилактических препаратов. Или подойти к Д.К. Львову, который с удовольствием расскажет про экологию любого вируса. Всегда открыт для общения и Ф.И. Ершов, который мгновенно изложит всю историю иммуномодуляторов и их влияние на любой компонент иммунной системы. В таких школах, живых и неформальных — наша сила. Они играют огромную роль в подготовке молодых кадров. Сейчас образовался довольно большой конкурс среди молодежи, желающей у нас работать, так что берем лучших.
Продолжается ли работа над другими проблемами или вы полностью переключились на COVID-19
Наш институт занят не только коронавирусом, есть и другие важнейшие направления, которые зачастую тесно связаны с данной проблематикой. Например, в результате массового попадания пациентов с этим заболеванием в стационары обостряется и без того наболевшая проблема внутрибольничных инфекций. Сейчас эта проблема стала кричащей. Массовое применение антибиотиков привело к тотальной резистентности микрофлоры, и большинство смертельных случаев связаны с сепсисом, когда к вирусной инфекции присоединяется бактериальная.
Одна из важнейших задач нашего времени — создание новых химиопрепаратов, которые преодолевают полирезистентность внутрибольничных штаммов и к которым не возникает такая резистентность.
Эта задача у нас успешно решается. Мы вышли на заключительную стадию клинических испытаний, которые проводим совместно с Городской больницей № 52, занимающейся спасением таких больных. Это работа школы Н. А. Зигангировой, которая возглавляет отдел медицинской микробиологии. Ею создано соединение, которое подавляет определенную мишень в так называемой третьей транспортной системе. Это фактор патогенности, который присутствует у большинства грамотрицательных бактерий, а они в свою очередь выступают основными переносчиками генов антибиотикорезистентности — главного бича внутрибольничных инфекций. В результате вышеупомянутой работы создано низкомолекулярное соединение, подавляющее эту третью транспортную систему, при этом не ограничивая размножение самой бактерии. Тем самым на эти бактерии не создается сильное эволюционное давление. Они не меняются, но перестают размножаться, в результате иммунная система благодаря фагоцитозу убивает такие бактерии. Подобные исследования не менее актуальны, чем создание вакцинного препарата, поэтому мы также выдвигаем Н.А. Зигангирову в Российскую академию наук.
Александр Леонидович, есть ли в опасном мире вирусов какие-то загадки, которые вам хотелось бы разгадать в первую очередь?
Этих загадок великое множество. Весь мир вирусов — сплошная загадка. Логистика поведения вирусов внутри клетки совершенно неясна. Как все это работает на самом деле, мы не знаем, можем лишь предполагать. Если проводить аналогию с железной дорогой, то это составы, принципы движения которых непонятны, и нет умных стрелочников, которые могли бы переключать стрелки. Если понимать всю логистику на молекулярном уровне, можно было бы создать лекарства от всех внутриклеточных патогенов, эффективные и безопасные, способные защищать нас от самых тяжелых заболеваний, включая онкологические.
Можно ли сказать, что, поняв логистику поведения вирусов, мы познаем мир?
Молекулярный мир — пожалуй, да.
А такое возможно?
Вряд ли такое произойдет при моей жизни, но последующим поколениям, уверен, это удастся. Для того и работаем.
Беседовала Наталия Лескова
Александр Леонидович Гинцбург, академик РАН, директор Национального исследовательского центра эпидемиологии и микробиологии им. Н.Ф. Гамалеи