Исследователи из Сколтеха, Уральского федерального университета и Института физики металлов имени М.Н. Михеева УрО РАН представили фундаментальное теоретическое описание важных свойств химической связи в материалах, предложив способ определения атомных зарядов и выделения ионной и ковалентной составляющих в энергии химической связи. Выводы учёных служат убедительным обоснованием традиционных представлений о химической связи, основанных на понятии электроотрицательности. Однако в ходе исследования был выявлен и противоречащий химической интуиции аномальный случай в виде полупроводникового соединения — фосфида бора. Результаты исследования опубликованы в журнале The Journal of Chemical Physics.
С начала XX века учёные пытались объяснить свойства молекул и кристаллов через химическую связь — свойство атомов притягиваться друг к другу за счёт перераспределения внешних электронов. Было установлено, что существуют различные типы связей. Например, при ковалентной связи два атома делят между собой общую электронную пару, которая и удерживает их вместе. Впоследствии оказалось, что атомов может быть не два, а больше. Такая связь между множеством атомов называется металлической. Известен и обратный случай, когда у двух атомов могут быть две и более общих электронных пар. В случае ковалентной полярной связи общая электронная пара смещается в сторону более электроотрицательного атома, и тогда образуются два противоположно заряженных иона, которые удерживаются вместе ионной связью.
«Рассмотрим связь, которая в материале удерживает атомы вместе. От степени ковалентности или ионности этой связи, или другими словами, от зарядов атомов, будет зависеть большинство свойств этого материала», — рассказывает соавтор исследования, руководитель Лаборатории дизайна материалов Сколтеха, заслуженный профессор Артём Р. Оганов. «Проблема в том, что за последнее столетие было предложено так много способов определения атомных зарядов, что до сих пор учёные не пришли к единому мнению о том, как это лучше делать и какие численные значения заряда считать корректными».
Существует ряд подходов, в которых атомный заряд определяют через свойства материала, которые поддаются измерению, например, количество энергии, затрачиваемой на разрыв связи. Другие подходы основаны на использовании математической операции интегрирования распределения электронной плотности по объёму атома, но и в этом случае однозначного определения пока не найдено. Существует также несколько подходов, где используются волновые функции атомов — базовые характеристики атомов в задачах квантовой механики. Здесь также существует множество способов анализа волновой функции, измерить которую непосредственно в эксперименте невозможно.
«В нашем методе, главным создателем которого является классик современной физики твёрдого тела Владимир Анисимов, используется формальное математическое описание так называемых функций Ванье, которые позволяют описать химическую связь в кристалле или молекуле на основе электронных орбиталей, максимально приближенных к атомным», — добавляет профессор Оганов. «С помощью нашего метода можно неэмпирическим путём определить атомные заряды и выделить ковалентную и ионную составляющие в энергии связи. Полученные результаты хорошо согласуются с химической интуицией. Исключением стал лишь кристалл фосфида бора, у которого атомные заряды оказались инвертированными».
Известно, что аналогичная картина инверсии наблюдается у молекулы угарного газа, состоящей из одного атома кислорода и одного атома углерода. Поскольку кислород обладает более высокой электроотрицательностью, чем углерод, логично предположить, что он будет сильнее притягивать к себе общую электронную пару: у кислорода возникнет частично отрицательный заряд, а у углерода — частично положительный. Однако в реальности происходит обратное. Похожая ситуация возникает и в случае атомов бора и фосфора, образующих кристалл фосфида бора ВР в соотношении один к одному. Несмотря на то что фосфор более электроотрицателен, чем бор, последний в итоге получает частично отрицательный заряд. Почему так происходит?
Этот феномен объясняется тем, что в обоих случаях невыгодный с энергетической точки зрения перенос электронов позволяет получить более прочную ковалентную связь, тем самым с лихвой компенсируя потери в энергии. В молекуле угарного газа из-за инверсии заряда образуется очень прочная тройная связь между кислородом и углеродом. Если бы атомы не пошли на эту «энергетическую жертву», то связь была бы только двойной. Таким же образом в фосфиде бора фосфор отдаёт один электрон бору, в результате чего у этих двух атомов оказывается по четыре валентных электрона, с помощью которых они создают ковалентные связи с соседями по кристаллической структуре. В противном случае и у бора, и у фосфора было бы всего по три связи на атом, что с энергетической точки зрения менее выгодно.
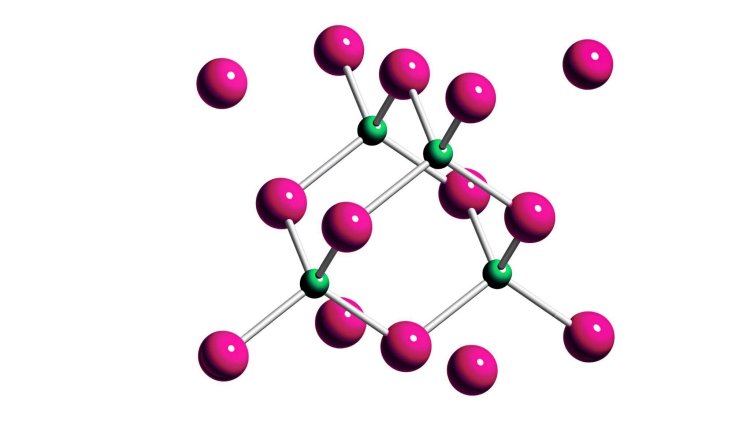
В кристалле фосфида бора каждый атом имеет связи с четырьмя соседними атомами. В отсутствии инверсии заряда у атомов было бы только по три связи. Авторы исследования предложили принципиально новую теоретическую модель, позволяющую учесть инверсию заряда. Изображение создано нейросетью Deep Dream Generator / предоставлено пресс-службой Сколтеха
Любопытно, что инверсия заряда в фосфиде бора была предсказана ещё двадцать лет назад в так называемых динамических зарядах Борна, которые с физической точки зрения имеют совершенно иную природу.
Предложенный учёными метод универсален, а значит, он поможет лучше понять характер химической связи в самых разных химических соединениях.
Исследование поддержано грантом Российского научного фонда № 19-72-30043.
Информация и изображение предоставлены пресс-службой Сколтеха