Аммиак — химическое вещество, необходимое для многих сельскохозяйственных и промышленных процессов, но его производство требует невероятно высоких энергетических затрат. Впервые группа исследователей из Токийского университета соединила атмосферный азот, воду и солнечный свет и, используя два катализатора, произвела значительное количество аммиака без высоких энергетических затрат. Новый метод, опубликованный в журнале Nature, отражает естественные процессы, происходящие в растениях с помощью симбиотических бактерий.
Вы наверняка слышали об аммиаке, особенно в связи с сельским хозяйством, где он является важным компонентом удобрений, питающих культуры, от которых зависит наша жизнь. Вот несколько цифр, которые помогут понять, почему аммиак имеет огромное значение: ежегодно производится 200 миллионов тонн аммиака, и 80% из них используется для производства удобрений. Кроме того, на его производство приходится около 2% всего мирового потребления энергии и, соответственно, около 2% мировых выбросов углекислого газа. Учитывая все это, понятно, почему исследователи по всему миру пытаются создать более чистый и эффективный способ производства аммиака.
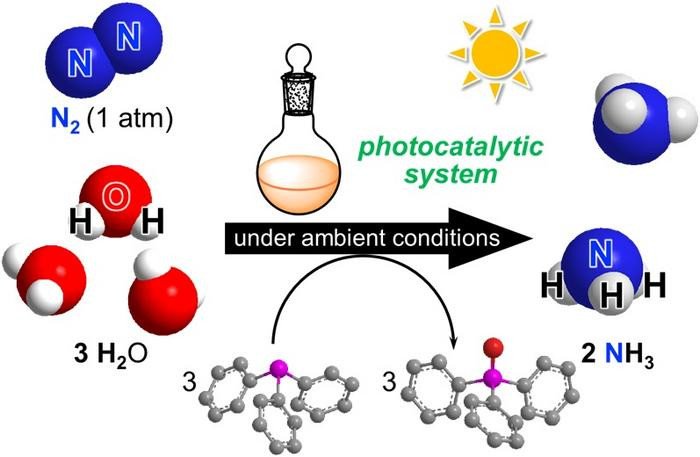
Профессор Йошиаки Нишибаяси с факультета прикладной химии Токийского университета и его команда недавно добились значительных успехов в достижении этой цели. Им удалось разработать новую каталитическую систему для получения аммиака из распространенных на Земле молекул, включая атмосферный азот и воду. Ключ заключается в комбинации двух видов катализаторов — промежуточных соединений, которые позволяют ускорить реакцию, не влияя на конечный продукт, созданных специально для производства аммиака и работающих под действием солнечного света.
«Это первый успешный пример фотокаталитического производства аммиака с использованием атмосферного динитрогена в качестве источника азота. И воды в качестве источника протонов, в котором также используется энергия видимого света и два вида молекулярных катализаторов», — говорит Нишибаяси. «Мы использовали иридиевый фотокатализатор и еще один химикат, называемый третичным фосфином, который позволяет фотохимически активировать молекулы воды. Эффективность реакции оказалась выше, чем ожидалось».
Дело в том, что химические реакции не всегда протекают так быстро, как вы хотите. И чтобы контролировать результат, эффективность и время процесса, необходимо задействовать дополнительные компоненты, помимо исходных ингредиентов. Вот тут-то и приходят на помощь катализаторы. Нишибаяси и его команда использовали два катализатора для этих экспериментов: один на основе переходного металла молибдена для активации динитрогена, а другой на основе переходного металла иридия для фотоактивации третичных фосфинов и воды. Третий компонент, называемый третичными фосфинами, также является ключом к тому, чтобы помочь извлечь протоны из молекул воды.
«Когда иридиевый фотокатализатор поглощает солнечный свет, его возбужденное состояние может окислить третичные фосфины. Затем окисленные третичные фосфины активируют молекулы воды путем образования химической связи между атомом фосфора фосфина и водой, в результате чего образуются протоны», — говорит Нишибаяси. Молибденовый катализатор позволяет азоту соединяться с этими протонами и превращаться в аммиак. Использование воды для получения дигидрогена или атомов водорода — один из важнейших процессов для достижения экологичности производства аммиака.
Команде удалось провести эту реакцию в масштабах, в 10 раз превышающих предыдущие эксперименты, что позволяет предположить, что она готова к испытаниям в более крупных масштабах, хотя все еще остаются некоторые вопросы, которые могли бы повысить безопасность и эффективность. Некоторые компоненты, такие как третичные фосфины, могут быть получены с помощью солнечной энергии или переработаны из оксидов фосфина. И хотя сами по себе они стабильны, при попадании в организм человека они могут быть токсичны, поэтому было бы идеально найти безопасный способ их утилизации или переработки.
«В растениях аммиак образуется в результате биологической фиксации азота с помощью цианобактерий и связан с фотосинтезом», — говорит Нишибаяси. «В этом случае электроны для реакции поступают от фотосинтеза, а протоны — из воды. Поэтому результаты нашего исследования можно рассматривать как успешный пример искусственного фотосинтеза аммиака».