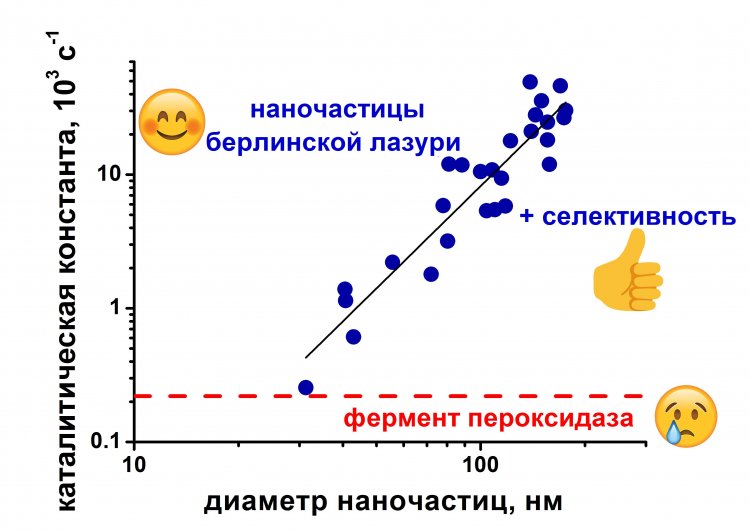
Ученые-химики МГУ разработали нанозимы (наночастицы, имитирующие природные ферменты), не уступающие по селективности и превосходящие по активности природную пероксидазу. Синтезированные наночастицы – единственные из нанозимов, которые могут найти применение в медицинской диагностике.
Пероксидаза, катализирующая восстановление пероксида водорода, является самым распространенным ферментом, используемым в качестве метки в иммуно-ферментном анализе. Поэтому имитирование пероксидазной активности, в частности, с использованием наночастиц, вызывало и вызывает большой интерес. Зарубежными учеными были созданы нанозимы, имитирующие пероксидазную активность, на основе платины. Однако как каталитическая активность, так и селективность (способность катализировать восстановление пероксида водорода в присутствии кислорода) у таких наночастиц значительно ниже, чем у природного фермента.
Ученые МГУ синтезировали нанозимы на основе электрокатализатора, созданного ими 25 лет назад. Электрокатализатор, содержащий в своей основе гексацианоферрат железа – берлинскую лазурь, как по каталитической активности, так и по селективности превосходит платину в 1000 раз.
Результаты научной работы, в которой российские химики предложили новый метод каталитического синтеза, позволяющий получить наночастицы, превосходящие по активности природный фермент пероксидазу, обнародованы в самом престижном рецензируемом химическом издании Journal of the American Chemical Society (JACS) от 2018, 140(36), рр.11302-11307.
На фото - первый автор статьи JACS, кандидат химических наук, старший научный сотрудник Мария Комкова и профессор Аркадий Карякин
Что такое нанозимы, почему интерес учёных вызвала соль берлинской лазури, и в чём состоит превосходство синтезированных из неё нанозимов по сравнению с природным аналогом – рассказал Аркадий Аркадьевич Карякин - доктор химических наук, профессор кафедры аналитической химии химического факультета МГУ имени Ломоносова.
«Антитела – это биомолекулы, которые синтезируются любыми организмами в ответ на появление каких-либо чужеродных агентов. Особенность антител в том, что у них очень высокая специфичность и очень высокое сродство к тому, на что они выработаны, – сообщил профессор Карякин и далее подробно пояснил, – Проблема состоит в том, как получить ответ: как создать биосенсоры на основе этих разных молекул. Если мы возьмем ферменты, то всё достаточно просто: там есть исходные вещества и есть продукты реакции. Можно по исходным веществам или по сопряженным продуктам реакции увидеть сигнал, что реакция идет. В случае антител это сделать невозможно, для них необходимы метки. Одной их самых популярных таких меток является пероксидаза. Мы попытались имитировать активность пероксидазы: вместо неё использовать наночастицы. Это намного порядков дешевле и на много порядков стабильнее».
Профессор Карякин занимается изучением биосенсоров (разновидностью химических сенсоров, имеющих биологическую систему распознавания) с 90-х годов прошлого века. Первые его публикации по созданию биосенсоров на основе берлинской лазури относятся к 1994-1995 годам. В итоге, уникальные аналитические характеристики таких биосенсоров (чувствительность, селективность, эксплуатационная стабильность) обусловили их использование и для клинического анализа. «Берлинская лазурь - это материал, впервые примененный нами для создания биосенсоров. Он является высокоактивным катализатором», - подчеркнул профессор Карякин.
Цикл работ Аркадия Карякина по этой теме был отмечен в 2015 году самой престижной наградой МГУ: Премией имени М. В Ломоносова «За научную деятельность».
Действительно ли каталитическая активность созданных нанозимов превосходит естественные аналоги? «Это экспериментальный факт, – считает профессор Карякин и аргументирует далее – Фермент - это достаточно большая молекула, а активный центр, там, где происходит катализ реакции, очень маленький. И на молекулу фермента он один. А у наночастиц активных центров много. Что касается наших наночастиц, то перекись водорода, как было показано, может проникать внутрь наночастиц. Так что работает весь объем. Поэтому, строго говоря, если пересчитать на один активный центр, конечно фермент может работать эффективнее. Но в сумме активность наночастиц на несколько порядков выше активности фермента».
Говоря об уникальности синтезированных наночастиц берлинской лазури, профессор Карякин, отметил: «Нам удалась сделать аналог фермента, который обладает не только высокой активностью, которая превосходит известные нам частицы по активности, но и высокой селективностью. Никакие наночастицы такой селективностью не обладают. Это единственные нанозимы, которые, как нам кажется, найдут применение в медицинской диагностике».
Экспериментальные исследования проходили в течение 2 лет в лаборатории химического факультета Московского государственного университета.
Каковы дальнейшие планы относительно синтезированных наночастиц берлинской лазури? «Первое – самое главное их использовать в качестве метки в иммуно-ферментном анализе и ДНК-зондах. Как уже было сказано, созданные нанозимы активнее фермента пероксидазы, а также гораздо дешевле и на много порядков стабильнее. Так что замена фермента на нанозимы, кроме улучшения характеристик диагностических наборов, должна дать и вполне серьезный экономический эффект. Кроме высокой каталитической активности, наночастицы берлинской лазури обладают очень высоким коэффициентом оптического поглощения, – ответил Карякин и пояснил затем – Поэтому их можно использовать не только как каталитическую, но и как оптическую метку. Этот материал намного дешевле используемых сегодня наночастиц золота, и коэффициент поглощения намного выше».
Российский химик признался, что упомянутая публикация вызвала интерес как в нашей стране, так и за рубежом. Сразу после выхода публикации пришел запрос из Института биофизики Пекина (КНР) о проведении совместных работ. В нашей стране работа уже нашла отклик среди специалистов в области иммуно-ферментного анализа из Кардиоцентра и Института биохимии РАН.