Коллектив сотрудников биологического факультета МГУ и НИИ физико-химической биологии имени А.Н. Белозерского МГУ предложил удобный метод для исследования механизма действия ингибиторов поли(АДФ-рибозо)полимеразаы (PARP), основанный на электрофорезе в полиакриламидном геле. PARP является ключевым белком репарации ДНК, а его ингибиторы представляют интерес в качестве инновационных противоопухолевых препаратов. Некоторые из них одобрены для лечения рака молочной железы и яичников, например олапариб (торговое название Lynparza). Предложенный метод позволяет описать механизм клинических ингибиторов олапариба, талазопариба и велипариба, а также новых, разрабатываемых в МГУ ингибиторов PARP. Работа выполнена в рамках НОШ МГУ «Молекулярные технологии живых систем и синтетическая биология» и опубликована в журнале «Вестник Московского университета».
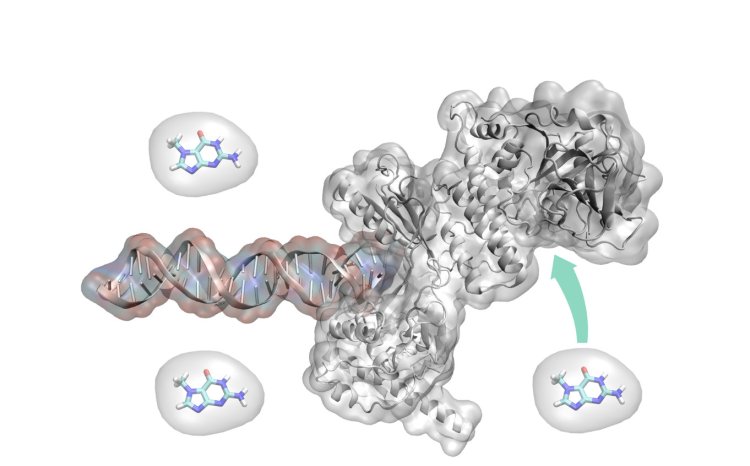
Общий вид молекулы PARP в комплексе с ДНК, вокруг показаны отдельные молекулы ингибитора. Источник: Дмитрий Нилов, НИИ физико-химической биологии имени А.Н. Белозерского МГУ
Ингибиторы PARP могут действовать различным образом, например, блокировать связывание PARP с поврежденной ДНК и/или подавлять синтез сигнального полимера в активном центре PARP, который необходим для привлечения других белков репарации к месту повреждения. При разработке лекарственного препарата следует иметь четкое представление о молекулярном механизме его действия. Например, в МГУ создаются ингибиторы PARP на основе 7-метилгуанина, для рационального дизайна которых необходимо знать участок связывания на поверхности белка или ДНК, и предложенный метод как раз помогает решать подобные задачи.
«Наш подход, основанный на электрофорезе в полиакриламидном геле, позволяет исследовать влияние ингибиторов как на ДНК-связывающую, так и на каталитическую активность белков PARP1 и PARP2, помогает определить участок связывания ингибитора», – отмечает сотрудник биологического факультета МГУ Ангелина Лобанова.
«Метод прост, надежен и может быть воспроизведен практически в каждой биохимической лаборатории», – добавляет доцент кафедры биоинженерии биологического факультета МГУ Наталия Малюченко.
Для активации PARP используется короткая двуцепочечная ДНК, имитирующая повреждение нативной ДНК. Далее анализируется электрофоретическая подвижность ДНК и ее комплексов с PARP. При взаимодействии PARP с ДНК наблюдается образование комплексов в виде дополнительных полос. При добавлении субстрата (НАД+) PARP начинает синтезировать отрицательно заряженный полимер, что приводит к электростатическому отталкиванию от ДНК и диссоциации комплексов PARP–ДНК (исчезновение полос). При добавлении ингибитора анализируется эффект на образование/исчезновение дополнительных полос и делается вывод (i) о влиянии на связывание PARP с ДНК и (ii) о влиянии на каталитическую активность PARP.
В результате удалось охарактеризовать действие известных ингибиторов PARP олапариба, талазопариба и велипариба, используемых в клинической практике. Например, было показано, что велипариб может препятствовать образованию комплекса PARP с ДНК. Также был протестирован ряд новых, разработанных в МГУ ингибиторов PARP на основе 7-метилгуанина.
«Нашей группой создается отечественный противоопухолевый препарат на базе ингибиторов PARP. Предложенный метод позволяет оперативно оценить ингибиторный потенциал и выбрать наиболее перспективные молекулы среди синтезированных соединений», – комментирует Дмитрий Нилов, ведущий научный сотрудник НИИ физико-химической биологии имени А.Н. Белозерского МГУ.
Информация и фото предоставлены пресс-службой МГУ