Сибирские ученые разработали универсальную платформу с использованием генетически кодируемых биосенсоров, которая позволит изучать механизмы возникновения различных патологий в режиме реального времени на клеточных линиях человека, сообщает издание «Наука в Сибири». В перспективе это пригодится в поиске терапии для широкого спектра заболеваний, в том числе тех, которые на сегодняшний день считаются неизлечимыми. Статья об этом опубликована в журнале Biochemistry (Moscow).
«Для моделирования различных патологических состояний используются индуцированные плюрипотентные стволовые клетки (ИПСК), — комментирует аспирантка лаборатории эпигенетики развития ФИЦ “Институт цитологии и генетики СО РАН” Елизавета Ивановна Устьянцева. — Фактически это аналоги эмбриональных стволовых клеток, только полученные искусственным путем. Главная особенность ИПСК — их плюрипотентность, то есть способность образовывать все типы клеток живого организма. Мы можем в условиях лаборатории заставить клетки вспомнить исходное состояние (как в эмбрионе), когда они еще не дифференцировались, то есть не выбрали определенную функцию в организме. Чтобы перепрограммировать клетки, необходимы специфические методы по активации в них спящих генов».
Ученые по всему миру создают ИПСК в лабораториях, но до сих пор не было разработано общепринятых стратегий их использования для биомедицинских задач. Основной сложностью работы с клеточными моделями остается поиск подходящего метода для измерения степени выраженности того или иного патологического процесса.
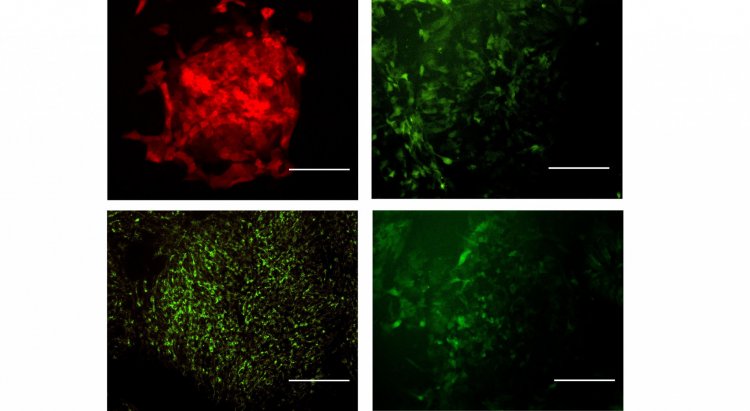
Для мониторинга внутриклеточных процессов и активности ферментов в режиме реального времени новосибирские биологи предложили использовать генетически кодируемые биосенсоры. «Они представляют собой специфические молекулы, в нашем случае флуоресцентные, которые под действием тех или иных стимулов меняют свои свойства. Активируя биосенсоры в больных и здоровых клетках, мы можем смотреть по каким параметрам они отличаются», — говорит Елизавета Устьянцева.
Биосенсоры встраиваются в геном клеток с помощью технологии геномного редактирования CRISPR/Cas9. «Раньше сенсоры помещались в клетки случайным образом, и была велика вероятность того, что работа генома могла нарушиться и исказить результаты исследования. Новый подход не влияет на функционирование клетки и на интерпретацию результатов, поскольку последовательность биосенсора прицельно встраивается в нужное, самое безопасное место генома», — поясняет Елизавета Устьянцева.
Задача ученых — оценить влияние определенных молекул на развитие заболевания. В частности, в своей статье они рассматривают патологические процессы, связанные с боковым амиотрофическим склерозом (БАС).
Исследования проводятся на двух клеточных линиях: полученной от пациента с мутацией, приводящей к развитию БАС, и здоровой — контрольной. «На основе этих линий ИПСК (в процессе репрограммирования их получается несколько) мы создали панель из пяти “больных” и пяти “здоровых” трансгенных клеточных линий, которые имеют один источник, но отличаются последовательностью биосенсора, встроенного в геном», — рассказывает исследовательница.
Биосенсоры позволяют наблюдать за процессами, характерными для нейродегенерации: окислительным стрессом (степень его выраженности может быть оценена косвенно через определение уровня содержания в цитоплазме перекиси водорода — промежуточного продукта в реакциях утилизации активных форм кислорода), апоптозом (степень его выраженности определяется активностью одной из эффекторных каспаз 3 — фермента, играющего ключевую роль в процессе программируемой клеточной гибели), а также стрессом эндоплазматического ретикулума (ЭПР) (этот процесс запускается в ответ на накопление патологических белков в клетке). «Мы надеемся, что метод позволит нам увидеть достаточно четкую разницу между больными и здоровыми клетками и удостовериться в том, что модель заболевания, которую мы создали на основе ИПСК, действительно подходит для изучения БАС», — говорит Елизавета Устьянцева.
Поскольку патологические механизмы, лежащие в основе различных нейродегенеративных заболеваний, во многом схожи, и те же самые процессы (окислительный стресс, стресс ЭПР, гибель клеток посредством апоптоза) наблюдаются и при других заболеваниях, платформу можно также использовать для поиска лекарств от спинальной мышечной атрофии, болезней Паркинсона, Альцгеймера, Гентингтона и прочих. Исследования проводятся на стволовых клетках, выделенных из периферической крови людей, поэтому в качестве посредников может выступать широкий пул медицинских центров, проводящих диагностику: предоставлять материал для получения ИПСК с генотипом пациента (с его обязательного информированного согласия). Процедура забора крови знакома людям и обычно не вызывает дискомфорта.
«В будущем такую систему можно применять для тестирования потенциальных лекарств, — отмечает Елизавета Устьянцева. — Мы имеем клетки, которые расположены в разных лунках. Таких лунок можно нарастить сотни, и в каждую капать какое-то действующее вещество и проводить массовый скрининг — смотреть, как изменились сигналы, получаемые от биосенсоров. Это поможет значительно сократить процесс поиска и отбора препаратов, направленных на лечение определенных заболеваний».
Исследовательница подчеркивает, что концепцию в перспективе можно развивать в более широких масштабах — использовать не только для мониторинга нейродегенеративных, но и других типов недугов, к примеру кардиологических, поскольку биосенсоры активно разрабатываются для широкого круга клеточных процессов.
В данный момент ученые готовят эксперимент по индукции образования в клетках активных форм кислорода, чтобы проверить, как клетки реагируют на этот параметр. «Мы уже владеем методикой направленной дифференцировки стволовых клеток in vitro в моторные нейроны — тип клеток, которые гибнут при БАС. В рамках нового эксперимента мы планируем активировать биосенсоры в больных и здоровых клетках и сравнить насколько сильно они реагируют на повышение концентрации активных форм кислорода. Это позволит узнать, отличаются ли показатели в моторных нейронах в стандартных условиях и в условиях стресса — при искусственно индуцированной болезни», — комментирует Елизавета Устьянцева.
Иллюстрация: Биосенсоры в клетках в работе/ Предоставлена Елизаветой Устьянцевой