Какой иммунитет эффективнее защищает от коронавируса, что будет после омикрона и как измерить Т-клеточный иммунитет с помощью кожного теста? На эти и другие вопросы в интервью «Научной России» ответил академик РАН, директор Санкт-Петербургского НИИ эпидемиологии и микробиологии имени Пастера Арег Артёмович Тотолян.
─ Расскажите, пожалуйста, о кожном тесте, разработанном в вашем Институте. Насколько я знаю, с его помощью можно измерить уровень специфического Т-клеточного иммунитета к коронавирусной инфекции, который сегодня в основном остается террой инкогнита.
─ Почему же террой инкогнита? О Т-клеточном иммунитете мы сегодня знаем уже немало. Но нюанс заключается в том, что оценка Т-клеточного иммунитета пока недоступна для нашего здравоохранения. Так сложилось, что оценка Т-клеточного иммунитета ─ это удел специализированных научных лабораторий, институтов, потому что необходимо особое дорогостоящее оборудование, дорогостоящие реактивы, специальная подготовка кадров, длительная процедура анализов и много других сложностей. Мы в Институте, проводя исследования Т-клеточного иммунитета на регулярной основе, пришли к выводу, что недостаточно судить о коронавирусной инфекции только по уровню антител или по наличию отсутствию вируса в ПЦР-анализе. Нужно еще и определение Т-клеточного иммунитета.
Член-корреспондент РАН А.С. Симбирцев предложил идею постановки теста, аналогичного пробе Манту или туберкулинового теста ─ это всё разные варианты кожного теста, которые предназначены, например, для решения вопроса, есть ли иммунитет к микробактерии туберкулеза или нет. Та же логика была использована и у нас. Новый кожный тест показывает, нужна ли вакцинация или нет. При этом учитываются не только Т-клеточный иммунитет, но и наличие антител в организме.
Справка. Антитела ─ не единственное средство защиты нашего организма от инфекций. Большую роль играет клеточная ветвь иммунитета, представленная Т-лимфоцитами. Это живые клетки крови, которые распознают зараженную вирусом клетку и уничтожают ее, таким образом прерывая цепочку распространения вируса.
Источник: Минздрав России. Иллюстрация: donfiore / 123RF
Тест очень простой. По сути, это аналог туберкулинового теста, но принципиальное отличие здесь заключается в использовании того антигена, который применяется для внутрикожного введения. Этот тест работает как в случае оценки постинфекционного иммунитета, так и для поствакцинального.
Заслуга группы А.С. Симбирцева заключается в создании гибридного белка, который состоит из наиболее иммуногенных (прим., участки белка, на которые прежде всего отвечает иммунная система) участков разных белков коронавируса. У всех на слуху М-белок и S-белок, но у коронавируса двумя белками дело не ограничивается: он гораздо сложнее устроен, там больше белков, и, соответственно, больше иммуногенных участков. Так вот, они собраны в единый достаточно большой гибридный белок, который вводится внутрикожно.
─ Это безопасно?
─ Он абсолютно не опасен для человека и не может вызвать заболевание. За счет того, что этот белок состоит из иммуногенных участков, как я уже сказал, мы можем увидеть, развивается иммунный ответ или нет, и оценить уровень Т-клеточного иммунитета. Соответственно, если результат отрицательный, и иммунного ответа нет, стоит задуматься о вакцинации.
Ответ на введение белка мы оцениваем в течение 72 часов. Это достаточно долго, целых три дня. Но таковы законы иммунологии.
─ Когда можно будет внедрить эту разработку в практическое здравоохранение?
─ Мы уже прошли все доклинические испытания: и на биобезопасность, и на токсикологию, и на специфичность в эксперименте. Уже поданы документы в Минздрав России на получение разрешения на проведение клинического исследования. Сейчас мы активно ведем диалог с Минздравом, отвечаем на их вопросы, и надеемся в ближайшее время приступить к первой фазе клинических испытаний.
У нашей разработки довольно сложная процедура регистрации, несмотря на то, что сам тест, по сути, является диагностическим. Но в связи с тем, что белок вводится внутрикожно, то есть нарушаются кожные покровы, эту тест-систему нужно регистрировать как лекарственный препарат.
─ В России есть аналоги вашей разработке?
─ Нет, на сегодняшний день их нет.
─ Насколько точен такой кожный тест?
─ Кожный тест более физиологичен и дает меньше ложных результатов. Но нужно понимать, что стопроцентно информативного теста в принципе не существует. Любой тест обладает какой-то погрешностью. Однако кожные тесты более информативны, нежели тесты in vitro. Но минусы таких кожных тестов связаны с более сложной процедурой регистрации.
Кожный тест, разработанный в ФБУН НИИ эпидемиологии и микробиологии имени Пастера. Изображение предоставлено А.А. Тотоляном
─ На недавнем Совете РАН Науки о жизни вы говорили о том, что гибридный иммунитет, когда человек и переболел, и был вакцинирован, наиболее эффективен при коронавирусе. Расскажите об этом подробнее.
─ Приведу, пусть грубую, аналогию. Когда вы учили стихи в школе, то запоминали их с первого раза? Нет. Так же и здесь: повторение мать учения. Всегда считалось, что постинфекционный иммунитет, когда человек переболел сам, более качественный, нежели поствакцинальный. Это правило работает в отношении подавляющего большинства инфекций, но в случае с коронавирусом дело обстоит немного иначе, и гибридный иммунитет здесь действительно выигрывает.
Наверняка вы слышали о таком понятии как бустерная доза, или бустеризация. Она широко используется за рубежом, в том числе для мРНК-вакцин. То есть человек получает сначала полную вакцину, так называемая первичная вакцинация, а затем небольшие дозы (бустеры) в необходимом количестве, чтобы поддерживать свой организм на должном уровне защиты. Это уже успешно применяется, например, в Израиле. И сейчас, когда жители Израиля столкнулись с омикроном, они идут не по пути ревакцинации, а по пути бустеризации. Одной такой бустерной инъекции достаточно, чтобы подстегнуть специфический иммунный ответ.
─ Верите ли вы в то, что омикрон станет последним вариантом коронавируса?
─ События последних двух лет показали, что прогнозы в отношении коронавирусов ─ самое неблагодарное дело, и здесь очень легко промахнуться. Я думаю, на омикроне эволюция вируса не остановится. Но насколько опасными для человека будут новые варианты вируса и как они будут обходить иммунную систему ─ покажет время.
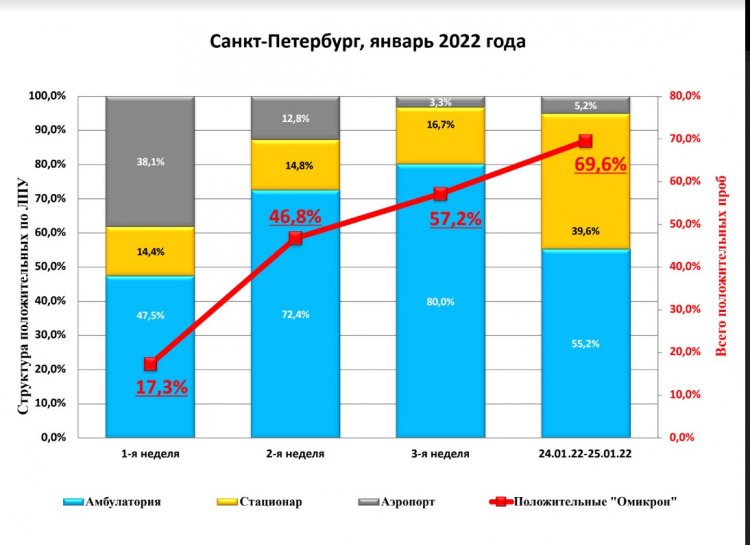
Судя по той динамике, которую мы сейчас наблюдаем в зарубежных странах, а также в Санкт-Петербурге и Москве, омикрон очень быстро завоевывает территорию и стремительно вытесняет дельту.
Рост количества заболевших омикроном в Санкт-Петербурге. Слайд предоставлен А.А. Тотоляном
─ Вы думаете, он вытеснит дельту полностью?
─ Вполне вероятно. Так же, как недавно дельта вытеснил предыдущие варианты вируса, сразу несколько геновариантов.
В Санкт-Петербурге в первой половине 2021 года циркулировали уханьский, британский, бразильский, южно-африканский штаммы и даже северо-западный ─ чисто российский геновариант. Кстати, этот вариант впервые был описан именно у нас в институте. В феврале мы его обнаружили и зарегистрировали в международной базе GISAID. Через месяц опубликовали эти данные. А в мае ВОЗ объявила его геновариантом, который необходимо наблюдать. Через неделю после этого объявления в Россию приходит дельта, и буквально у нас на глазах в течение трех недель практически исчезает северо-западный вариант, уходит британский и т.д. ─ всех вытеснил дельта. Первая дельта была зафиксирована в Санкт-Петербурге на майских праздниках, а в июле он вытеснил все остальные.
─ Вы говорите, что эволюция коронавируса на омикроне не остановится. Но, раз так много людей уже переболело, можно ли сказать, что наши организмы уже адаптировалось к коронавирусу и что последующие штаммы будут более легкими?
─ Нет, такие прогнозы строить невозможно. В том, что эволюция вируса будет продолжаться, никаких сомнений нет, а вот насколько он будет опасен, повторюсь, мы не знаем.
Чисто психологически после дельты мы все готовились к тому, что следующий вариант вируса будет еще опаснее. Тем не менее мы видим, что омикрон, хоть и намного быстрее распространяется, переносится легче, чем дельта. Конечно, есть случаи тяжелых форм и госпитализаций, но их не так много, как было с дельтой.
─ То есть эволюция коронавируса может пойти по абсолютно любому сценарию: следующий вариант может быть еще опаснее, а может и нет?
─ Все верно. Плюсы всей этой истории заключаются в том, что те, кто переболел одним вариантом коронавируса, например уханьским или дельтой, и, кроме того, сейчас еще омикроном, имеют больше шансов быть защищенными от последующего варианта вируса.
─ А если еще вакцинированы, так вообще красота: исходя из тезиса о том, что гибридный иммунитет лучше.
─ Да, чем богаче иммунный ответ, чем больше в арсенале иммунной системы специфических клеток, тем лучше.
Каждый новый вариант вируса, если он попадает в организм, оставляет о себе след в виде клеток памяти. И при повторной встрече с вирусом эти клетки памяти начинают работать на защиту организма. Так вот, чем разнообразнее специфичность этих клеток памяти, тем больше шансов, что последующие версии вируса будут протекать в менее тяжелой форме и человек будет к ним устойчив.