Ученые из Гарвардской медицинской школы и Бостонской детской больницы (США) улучшили метод редактирования генов CRISPR-Cas9, чтобы излечить мышей от наследственной глухоты – той же болезни, которая прогрессировала у знаменитого немецкого композитора Людвига ван Бетховена. Усовершенствованный инструмент позволил ученым отключить дефектную копию слухового гена Tmc1, сохранив при этом здоровую копию, пишут на сайте Гарвардской медицинской школы.
Новый подход, описанный онлайн в Nature Medicine, представляет собой оптимизированную, более точную версию классической системы редактирования генов CRISPR-Cas9: она лучше распознает вызывающую болезнь мутацию, которую ученые наблюдали у «мышей Бетховена». Как сообщают исследователи, их системе удалось найти один неправильный элемент – одну букву – ДНК в дефектной копии гена.
Каждый наследует две копии одного и того же гена – по одной от каждого родителя. Во многих случаях одного нормального гена достаточно, чтобы он правильно выполнял свою функцию, которая избавляет человека от болезни. Напротив, при так называемых доминантно наследуемых генетических расстройствах – как в случае с «болезнью Бетховена» – единственная дефектная копия может вызвать заболевание.
«Формула» гена, о котором идет речь, выглядит так: Tmc1. У мышей потеря слуха связана с одной неправильной буквой в последовательности ДНК этого гена: А вместо T. Эта маленькая, казалось бы, ошибка означает разницу между нормальным слухом и глухотой.
Чтобы сохранить слух животному, достаточно лишь отключить «бракованную» копию гена Tmc1. Но как это можно сделать безопасно, случайно не отключив и здоровый ген?
Два ключа лучше, чем один
Классические системы редактирования генов CRISPR-Cas9 работают с использованием направляющей молекулы гидовой РНК (gRNA), которая определяет последовательность мутантной ДНК. Как только ДНК-мишень точно определена, режущий фермент – Cas9 – отсекает ее.
Пока что эти генные редакторы работают не идеально. Это связано с тем, что направляющая РНК, которая ведет фермент Cas9 к мишени, и сам фермент Cas9, который разрезает ДНК, не совсем точны и могут в конечном итоге разрезать неправильную ДНК.
Чтобы обойти эти проблемы, исследователи адаптировали инструмент, первоначально разработанный Китом Джунгом (Keith Joung), профессором патологии в Гарвардской медицинской школе, и Беном Кляйнштивером (Ben Kleinstiver), доцентом кафедры патологии HMS в Массачусетской больнице общего профиля. Их инструмент использует модифицированный фермент Cas9, полученный из золотистого стафилококка, вместо стандартного Cas9, который обычно получают из стрептококка пиогенного.
Чтобы обеспечить точность системы, в ней объединили два уровня распознавания мишени: рРНК для определения местоположения гена-мишени и модифицированную форму Cas9, которая может точно определять специфическую мутацию ДНК у «мышей-Бетховенов». С помощью таких двух форм идентификации система точно находит дефектную копию и вырезает только ее, не замечая нормальную ДНК.
В первых экспериментах на клетках с «болезнью Бетховена» и без нее инструмент точно различал мутантную ДНК и нормальную ДНК в копиях гена Tmc1. Дальнейший анализ показал, что в клетках, которые содержали одну дефектную и одну нормальную копию гена, по меньшей мере 99% молекулярных «срезов» происходили исключительно в дефектной копии гена.
«Глушитель» глухоты
После первой удачи ученые перешли к экспериментам с мышами, которые страдали болезнью Бетховена и которые были здоровы. Анализ ДНК показал, что «редактура» была проведена только в клетках внутреннего уха у мышей с дефектом. У здоровых же грызунов никаких изменений редактирования ДНК не было обнаружено. Этот эксперимент подтвердил точность нового инструмента генной терапии.
Чтобы определить, влияет ли терапия редактирования генов на нормальную функцию генов, ученые стимулировали рецепторы слуха – так называемые волосковые клетки – во внутренних ушах здоровых грызунов. Клетки показали нормальные слуховые реакции, подтверждая, что терапия редактирования генов не повлияла на нормальную функцию генов.
Далее исследователи проверили у животных слух. Они измерили слуховые реакции ствола мозга мышей, которые фиксируют, какое количество звука обнаруживается волосковыми клетками во внутреннем ухе и передается в мозг.
«Мыши-Бетховены», которые не получили лечения при рождении, обычно полностью теряли слух к шести месяцам. Для сравнения, мыши без генетического дефекта сохраняют нормальный слух на протяжении всей жизни и могут слышать звуки на уровне около 30 децибел – примерно с такой громкостью мы шепчем.
А вот у тех грызунов, которых лечили, уже через два месяца после терапии слух заметно улучшился. Эти животные были способны обнаруживать звуки на уровне 45 децибел – уровень громкости нормального разговора. То есть примерно они слышат примерно в 16 раз лучше, чем мыши без лечения. В целом мыши, у которых «отключили» мутантную ДНК, могли слышать звуки в диапазоне от 25 до 30 децибел. Их слух почти не отличался от слуха здоровых сверстников. У некоторых мышей слух оставался на таком же стабильном уровне в течение года.
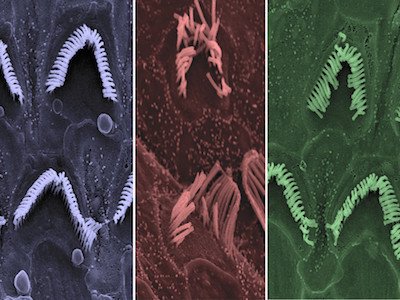
При «болезни Бетховена» слуховые клетки во внутреннем ухе теряют свою структуру и гибнут. Ученые решили проверить состояние этих клеток у мышей после генной терапии. Как и ожидалось, у мышей, не получивших лечение, слуховые клетки теряли свою структуру и гибли. У здоровых же или у вылеченных мышей количество слуховых клеток не менялось.
В последнем эксперименте ученые проверили эффект лечения в линии человеческих клеток, несущих «мутацию Бетховена». Анализ ДНК показал, что терапия вызывала редактирование исключительно в мутантной копии гена Tmc1 и не повлияла на нормальную копию.
Однако исследователи спешат предупредить, что еще предстоит проделать большую работу, прежде чем даже очень точную генную терапию, подобную их методу, можно будет применять на людях. Тем не менее, работа представляет собой важный этап, поскольку она значительно повышает эффективность и безопасность стандартных методов редактирования генов.
«Наши результаты показывают, что эта версия уже классического инструмента редактирования CRISPR/Cas9 достигает беспрецедентного уровня идентификации и точности», – сказал соавтор исследования Дэвид Кори (David Corey), профессор в области трансляционной медицины из Института Блаватника при Гарвардской медицинской школе.
Кроме того, по словам команды, на основе этого исследования можно разработать точный подход для лечения других доминантно наследуемых генетических заболеваний, которые возникают из-за одной дефектной копии гена.
На изображении слева направо: волосковые клетки здоровых мышей, клетки мышей, теряющих слух и не получивших лечение, клетки больных мышей, чью ДНК отредактировали с помощью нового инструмента.
[Фото: Carl Nist-Lund and Jeffrey Holt]