Изображение: Kostya Kartavenka, Flickr, Creative Commons
В тяжелой воде все атомы обычного водорода (протия) замещены на атомы его более тяжелого изотопа - дейтерия. Ее применяют в качестве замедлителя нейтронов в ядерных реакторах, а сам дейтерий необходим для проведения управляемого термоядерного синтеза и во многих других научных и прикладных задачах. Но, несмотря на стратегическое значение тяжелой воды, ее не производят в России, и запасы тяжелой воды стремительно сокращаются. Российские ученые из РХТУ им. Д.И. Менделеева и АО ВНИИНМ им. А.А. Бочвара нашли способ управлять структурой и за счет этого свойствами платинового катализатора, необходимого для ключевого этапа получения тяжелой воды. Результаты работы опубликованы в журнале Fusion Engineering and Design, а новые катализаторы, по словам ученых, хорошо подходят не только для синтеза тяжелой воды, но и, например, для аварийного окисления водорода на атомных электростанциях.
Физико-химические свойства тяжелой воды практически не отличаются от обычной, но ее ядерные и биологические свойства отличаются кардинально. Следовые количества дейтерия есть в абсолютно любой воде, а его абсолютная концентрация зависит от природных условий в месте ее происхождения. Так, за счет жаркого и сухого климата концентрация дейтерия в соке египетских апельсинов заметно выше, чем, например, в вологодском молоке. Однако этого различия недостаточно для решения промышленных задач.
Впервые получать тяжелую воду научились еще в начале XX века с помощью электролиза воды. Этот метод сравнительно прост, но очень энергозатратен, и поэтому его постепенно применяли всё меньше и меньше. Сейчас одним из самых эффективных считают метод с использованием реакции химического изотопного обмена, в которой атомы дейтерия из одного соединения меняются местами с обычными атомами водорода другого соединения. Большая часть тяжелой воды в мире была получена по методу изотопного обмена в системе вода-сероводород, то есть дейтерий для обогащения воды извлекался из сероводорода, но из-за экологических проблем, связанных с высокой токсичностью сероводорода, большинство таких производств закрыто. А сейчас для получения тяжелой воды рассматривают систему вода-водород.
Этот процесс проводят в больших колоннах, где взаимодействуют потоки воды и водорода: из водорода извлекают дейтерий, которым обогащают воду. Обмен повторяется многократно, пока обычная вода не превратится в тяжелую. Ключевая стадия этого процесса проходит только в присутствии платинового гидрофобного катализатора, который можно получить двумя способами: либо взять уже гидрофобный по своей природе носитель (подложку для катализатора) и пропитать его раствором платины, либо использовать изначально гидрофильный носитель, поверхность которого сначала покрыть гидрофобным веществом (то есть гидрофобизировать), а уже потом нанести платину. Выбор типа катализатора зависит от производительности разделительной колонны и условий ее работы.
“К гидрофобизированному катализатору предъявляются противоречивые требования. С одной стороны, у него должна быть гидрофобная поверхность, иначе в процессе эксплуатации катализатора в колонне он покроется пленкой воды, и реакция на нем сразу перестанет идти. С другой стороны, нам необходимо нанести платину, которая собственно и катализирует реакцию изотопного обмена, но в процессе нанесения платины мы неизбежно нарушаем гидрофобность этой поверхности, - рассказывает один из авторов работы, доцент РХТУ Алексей Букин. - Достижению этого компромисса и была посвящена наша работа. Мы изменяли условия нанесения платинового покрытия и смотрели, как с помощью них можно управлять свойствами катализатора, чтобы в конечном счете сделать его более совершенным”.
Установки для электролизного получения тяжелой воды. Изображение: martin_vmorris/Flicrk
Заглянуть под оболочку
В новой работе исследователи использовали в качестве носителя катализатора сферические гранулы оксида алюминия Al2O3. Их поверхность изначально гидрофильна, и поэтому ее покрывали гидрофобным слоем термостойкого кремнийорганического соединения. Дальше на эту гидрофобную поверхность уже наносили платину, используя для этого гексахлорплатиновую кислоту с добавками других кислот - в одном случае это была соляная, в другом щавелевая, а в третьем никаких дополнительных кислот не использовали.
Потом ученые оценивали гидрофобность полученных катализаторов и их каталитические свойства. Оказалось, что гидрофобность поверхности гранул всех трех образцов примерно идентична, а их каталитические свойства, наоборот, отличались. Лучше всего показал себя катализатор, нанесенный из чистого раствора гексахлорплатиновой кислоты, а добавки других кислот приводили к ухудшению свойств образцов.
Чтобы объяснить такое поведение, ученые изучили состав гранул катализатора. Оказалось, что во всех образцах при движении от ядра гранул к поверхности уменьшалось содержание кремния, что говорит о частичном разрушении гидрофобного кремнийорганического покрытия. Эта особенность оставалась неизменной для всех образцов, а вот характер распределения платины внутри катализатора, наоборот, изменялся: в одних образцах она в основном выходила на поверхность, а в других высокая концентрация собиралась, например, еще в ядрах гранул. Такие различия в структуре гранул напрямую коррелировали с их каталитическими свойствами. В дополнительных экспериментах авторы установили предельное содержание кремния, при котором гранулы еще сохраняют свои гидрофобные и, как следствие, каталитические свойства - эта величина составила 2%.
“В этой работе мы предложили инструмент для того, чтобы наблюдать, как распределяется платина внутри катализатора, и одновременно контролировать гидрофобность покрытия. Теперь, вооруженные этими методами, мы можем разрабатывать новые, более эффективные катализаторы, - рассказывает Алексей Букин. - Это заметно расширяет диапазон и область применения гидрофобизированных катализаторов изотопного обмена”.
Исследователи подчеркивают, что если получение тяжелой воды организовать на предприятиях по промышленному производству водорода, то это повысит конкурентоспособность системы вода-водород по сравнению с другими методами. Такими предприятиями могут стать атомные электростанции - на них планируют производить много водорода, из которого тут же можно будет получать тяжелую воду. Полученные в ходе исследования результаты могут быть использованы для наработки промышленной партии катализатора.
Кроме того, платиновые гидрофобизированные катализаторы можно применять и для других процессов с участием водорода. Так, высокая термостойкость катализаторов позволит использовать их на атомных станциях для аварийного окисления больших количеств водорода. Контролируемое нанесение платины позволит увеличить срок службы таких катализаторов, а следовательно, повысить безопасность процесса.
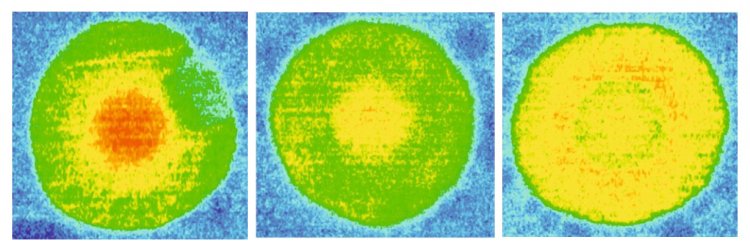
Распределение изотопной метки трития по сечению катализатора. С помощью этого измерения дополнительно изучали, как состав гранул определяет их каталитические свойства. Изображение предоставлено авторами исследования
Статья: V.S. Moseeva, Synthesis method of hydrophobic catalysts for the hydrogen activation with a controlled platinum distribution, Fusion Engineering and Design (Q2), 2021, DOI: 10.1016/j.fusengdes.2021.112571
Источник информации и фото: РХТУ им. Д.И. Менделеева