Группа ученых из Института интеллектуальных систем им. Макса Планка (Германия) добавила бактериям кишечной палочки искусственные компоненты, чтобы создать биогибридных микророботов. Такие биоботы помогут доставлять лекарства непосредственно к месту опухоли, сообщает пресс-служба института. Подробно разработка описана в журнале Science Advances.
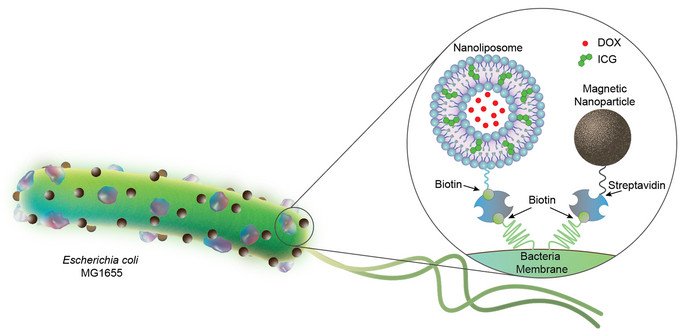
Команда прикрепила к каждой бактерии несколько нанолипосом – крохотных везикул сферической формы. По внешнему кругу они несут материал (ICG, зеленые частицы), который плавится под ближним инфракрасным светом. Ближе к середине, внутри ядра, липосомы инкапсулируют молекулы водорастворимых химиотерапевтических препаратов (DOX).
Второй компонент, который исследователи прикрепили к бактерии, — это магнитные наночастицы. При воздействии магнитного поля частицы оксида железа служат дополнительным усилителем для этого и без того очень подвижного микроорганизма. Липосомы и магнитные частицы связываются с бактерией «веревкой», которая представляет собой очень стабильный и трудно разрушаемый комплекс из белка стрептавидина и биотина, разработанный несколькими годами ранее.
Бактерии E. coli — быстрые и универсальные пловцы, которые могут перемещаться как в жидкостях, как и в очень вязких тканях. Кроме того, они обладают высокоразвитыми сенсорными возможностями. Бактерии «привлекают» химические градиенты, такие как низкий уровень кислорода или высокая кислотность, которые преобладают вблизи опухолевой ткани.
Эксперименты показали, что микророботы на основе E. coli могут пробраться через среду с высокой плотностью – как опухолевая ткань – и достичь цели. Сначала ученые провели их через Г-образный узкий канал с двумя отсеками на каждом конце, по одному опухолевому сфероиду в каждом. А после – через еще более узкую структуру, напоминающую крошечные кровеносные сосуды. Они добавили дополнительный постоянный магнит с одной стороны. С его помощью ученые смогли точно направлять микророботов, нагруженных лекарством, к опухолевым сфероидам. Далее команда провела микророботов через вязкий коллагеновый гель (напоминающий опухолевую ткань) с тремя уровнями жесткости и пористости, от мягкого до среднего и жесткого. Чем жестче коллаген, чем плотнее паутина белковых нитей – и тем труднее бактериям найти путь через матрикс. Но, как только добавляется магнитное поле, бактериям удается пройти весь путь до другого конца геля.
Когда микророботы собираются в нужной точке (сфероиде опухоли), лазер ближнего инфракрасного диапазона генерирует лучи с температурой до 55 градусов по Цельсию – и липосома плавится. В результате высвобождаются заключенные в липосоме лекарства. Низкий уровень pH или кислая среда также вызывают разрыв нанолипосом, поэтому лекарства автоматически высвобождаются рядом с опухолью.
Доставка лекарства с помощью подобных биороботов к месту опухоли была бы минимально инвазивной для пациента и безболезненной. Действие лекарств проявлялось бы там, где это необходимо, а не по всему организму, отмечают авторы работы.
[Иллюстрация: AKOLPOGLU ET AL., SCI. ADV. 8, EABO6163 (2022)]