При кортикоспинальных повреждениях мозга в мышиной модели взрослые нейроны начинают естественный процесс регенерации, возвращаясь к эмбриональному состоянию, и эта регенерация поддерживается удивительным геном, - пишет eurekalert.org со ссылкой на Nature.
Когда взрослые клетки мозга получают травмы, они возвращаются в зародышевое состояние, - выяснили исследователи из Калифорнийского медицинского университета в Сан-Диего совместно с коллегами из других стран. Ученые сообщают, что в зародышевом состоянии клетки способны повторно выращивать новые соединения, которые при правильных условиях могут помочь восстановить утраченную функцию.
Восстановление повреждений головного и спинного мозга может быть самой сложной задачей медицинской науки. До недавнего времени это казалось невыполнимой задачей. В новом исследовании изложена «транскрипционная схема регенерации в мозге взрослого человека».
«Используя невероятные инструменты современной нейробиологии, молекулярной генетики, вирусологии и вычислительной математики, мы впервые смогли определить, как весь набор генов во взрослой клетке мозга перезагружается для регенерации. Это дает нам фундаментальное понимание как на транскрипционном уровне происходит регенерация», - сказал старший автор Марк Тушински, доктор медицинских наук, профессор нейробиологии и директор Института трансляционной нейронауки Медицинского факультета Калифорнийского университета в Сан-Диего.
Используя модель мыши, Тушински и коллеги обнаружили, что после травмы зрелые нейроны в мозге взрослого человека возвращаются в эмбриональное состояние. «Кто бы мог подумать, - говорит Тушински. - Всего 20 лет назад мы думали о мозге взрослого как о статичном, окончательно дифференцированном, полностью сформировавшемся и неизменном».
Но работа Фреда "Расти" Гейджа - доктора философии, президента и профессора Института биологических исследований Солка и адъюнкт-профессора в Калифорнийском университете в Сан-Диего и других ученых, обнаружила, что новые клетки мозга на протяжении всей жизни появляются в гиппокампе и субвентрикулярной зоне.
«Наша работа еще более радикализует эту концепцию, - сказал Тушински. - Способность мозга восстанавливать или заменять свои клетки не ограничивается только двумя областями. Так, когда повреждена клетка коры головного мозга взрослого человека, она превращается (на уровне транскрипции) в эмбриональный кортикальный нейрон. И в этом обратном, гораздо менее зрелом состоянии, нейрон может вырастить аксоны, если ему предоставлена среда для роста. На мой взгляд, это самая выдающаяся особенность исследования и это просто шокирует».
Чтобы обеспечить «благоприятную среду для выращивания аксонов», Тушински и его коллеги исследовали, как поврежденные нейроны реагируют на повреждение спинного мозга. В последние годы исследователи значительно расширили возможности использования привитых нервных стволовых клеток для стимулирования восстановления травм спинного мозга и восстановления утраченной функции в основном путем побуждения нейронов расширять аксоны через место травмы, восстанавливая разрыв отрезанных нервов.
В прошлом году, например, междисциплинарная команда во главе с доктором наук Коби Коффлером, доцентом нейробиологии Тушински, и доктором наук Шаоченом Ченом описала использование 3D-печатных имплантатов для стимулирования роста нервных клеток при повреждениях спинного мозга у крыс, восстановления связей и потерянных функций.
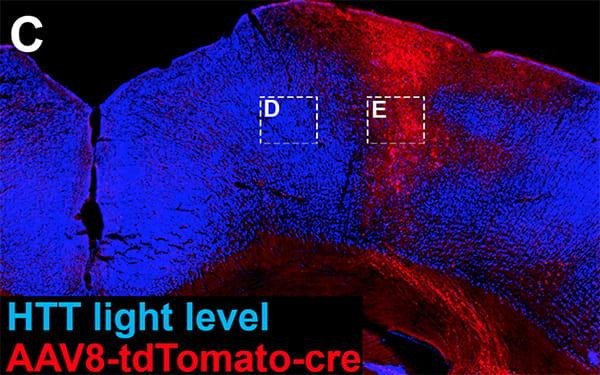
Последнее исследование подарило второй сюрприз: в стимулировании роста и восстановления нейронов один из важнейших генетических путей включает ген Хантингтина (HTT), который при мутировании вызывает болезнь Хантингтона - разрушительное расстройство, характеризующееся прогрессирующим разрушением нервных клеток в мозге.
Команда Тушински обнаружила, что «регенеративный транскриптом» - коллекция молекул РНК-мессенджера, используемых кортикоспинальными нейронами - поддерживается геном HTT. У мышей, генетически сконструированных с отсутствием гена HTT, после повреждения спинного мозга была снижена регенерация нейронов.
«Несмотря на то, что уже была проделана большая работа для
понимания, почему мутации Хантингтина вызывают заболевание,
гораздо меньше было известно о роли в этом Хантингтина, - сказал
Тушински. - Наша работа показывает, что Хантингтин необходим для
ускорения восстановления нейронов головного мозга. Таким образом,
можно было бы предсказать, что мутации в этом гене приведут к
потере способности взрослого нейрона к самовосстановлению. Это, в
свою очередь, может привести к медленной дегенерации нейронов,
что вызывает болезнь Хантингтона.
[Фото: eurekalert.org, ru.123rf.com/profile_ssilver]