В преддверии Нового года принято подводить итоги, отмечать самые яркие достижения в тех или иных областях науки, и эту добрую традицию не стоит отменять даже в столь непростые времена, как пандемия COVID-19.
Для врачей этот год выдался особенно сложным, ведь они работали и работают буквально на пределе своих возможностей. Несмотря на это, ученым за последний год удалось добиться серьезных результатов в самых различных областях знания. О наиболее ярких достижениях 2020 года в онкологии нам рассказал Андрей Дмитриевич КАПРИН — академик РАН, практикующий хирург, главный внештатный онколог Минздрава России, генеральный директор ФГБУ "НМИЦ радиологии" Минздрава России.
— Говоря о последних достижениях, нельзя не упомянуть такую тему, как Нобелевская премия, в этом году присужденная за так называемые генетические ножницы. Расскажите, пожалуйста, что это такое и можно ли эту технологию применять как-то в лечении рака?
— Эммануэль Шарпантье и Дженнифер Дудна — действительно великие люди. В этом году им присудили Нобелевскую премию по химию, и их открытие — способность некоторых молекул разрезать другие молекулы, — для нас, онкологов, имеет очень большое значение.
Чтобы предотвратить мутацию клетки, которая начинает в организме бесконтрольно делиться, мы рассчитываем использовать эту возможность влияния на ДНК, на репликацию рибонуклеиновых кислот, и не только предотвратить, а даже приостановить уже развившуюся клетку. Этот механизм должен помочь собственным клеткам уничтожить клетку-врага. Тем более мы знаем, что, к сожалению, раковые клетки имеют свойство довольно быстро приспосабливаться к любому состоянию, в том числе и к Т-киллерам, то есть они так мастерски маскируются, что собственные клетки организма их просто не распознают. И, если в нашей борьбе с раком будет такой инструмент, как генетические ножницы, то это здорово продвинет онкологию вперед.
Да, пока что это только проектное предложение, которое требует дальнейшей доработки, но все равно — это те самые важные первые шаги, позволяющие развить так называемую внутритканевую, клеточную хирургию. Может быть, эта технология позволит даже заранее влиять на эту опухолевую клетку у детей, имеющих предрасположенность к развитию рака.
Э. Шарпантье и Д. Дудна стали первыми, кто показал, что система CRISPR-Cas, которая используется бактериями для борьбы с вирусами-бактериофагами, может быть использована и для того, чтобы распознавать и "раскусывать" ДНК практически в любой заданной последовательности, то есть служить генетическими ножницами.
Источник фото: Nobelprize.org
— То есть до внедрения в практику еще далеко?
— Пока что да. А помните все предыдущие Нобелевские клеточные теории? Это еще пока даже не доклиника.
Понятно, что по результатам открытия Шарпантье и Дудны потом нужно еще будет проводить и доклинику, и клинику развивать. Это все дорогостоящие и большие исследования. Так что открытие сейчас носит сугубо теоретический характер, но эту технологию, я считаю, нужно обязательно использовать. А внедрение в клинику, в практику, в эксперименты – это тоже огромная работа, требующая больших затрат.
— Кстати, в этом году ведь была выполнена еще одна важная работа, связанная с генетикой, — секвенирование генома коронавируса...
— Да, это очень интересная отечественная работа. Учеными НИИ гриппа им. А.А. Смородинцева было проведено полное геномное секвенирование SARS-CoV-2, позволяющее оценить вообще происхождение этого вируса. И более того, может быть, такое глубокое секвенирование, нам даст возможность выйти на работу с онковакцинами. Потому что вот это вирусное генетически-мутационное развитие может позволить этот вирус потом применять в ослабленном виде как онколетиктическую вакцину. Результаты, полученные российскими учеными, были депонированы в международную базу данных EpiCoV GISAID, используемую ВОЗ и ведущими мировыми исследовательскими группами для мониторинга глобальной эволюции коронавируса.
— Возвращаясь к вопросу лечения рака, сейчас очень перспективное направление – адаптивная иммунотерапия. Расскажите, пожалуйста, о нем подробнее.
— Да, это адаптация собственного иммунитета, собственных иммунных клеток к той или иной среде. Как я уже говорил, собственный иммунитет не всегда различает раковую клетку. И, когда мы это делаем вне организма, когда мы забираем собственные иммунные клетки и учим их борьбе с раковыми клетками вне организма, — это направление представляется очень перспективным. Работы проводятся в том Центре, который мне доверено возглавлять: МРНЦ им. А.Ф. Цыба (филиал "НМИЦ радиологии" Минздрава России). Это происходит в городе Обнинске, который всегда славился своим научным потенциалом. Там у нас открыта специальная лаборатория, которая позволяет такие исследования проводить. В ходе лечения у пациента формируется и активируется противоопухолевый иммунный ответ за счет введения малых доз активированных иммунных цитоксических клеток донора, способных разрушить, убить опухоль.
Это крайне важно, ведь онкологическая клетка очень адаптивна. И есть еще одна проблема, которая всегда нас настораживает. Дело в том, что опухоль состоит из пула разных стволовых клеток. И, даже подобрав препарат иногда на весь «набор» стволовых клеток для воздействия с помощью CAR-T терапии, адаптивной иммунологии, все равно может остаться какая-то часть, к которой придется подбираться отдельно. Вот такое поразительное умение опухоли приспосабливаться, которое мы, к сожалению, наблюдаем.
— А сколько ей требуется времени, чтобы так хорошо приспособиться в организме?
— Вы знаете, очень по-разному. Например, иногда, когда мы действуем даже очень хорошими препаратами, самыми чистыми, но в то же время самыми агрессивными, у некоторых пациентов через полгода-год возникает резистентность к химиотерапии.
А есть, например, наблюдение, когда гормонорезистентность у одних пациентов возникает через два-три месяца, а у некоторых — даже при воздействии в течение нескольких лет и при не постоянном воздействии, а так называемых прерывистых курсах лечения, — не возникает вообще. Сегодня мы, онкологи, вооружены достаточно хорошо: имеем и генетический сиквенс, и молекулярное исследование клетки, чтобы видеть, в том числе, ее готовность к быстрому метастазированию, к достаточно резкому прогрессированию (показатель так называемой степени злокачественности опухоли клетки). Мы наблюдаем и так называемые процессы замирания, затухания, то есть довольно длительные периоды стабилизации.
— Какие достижения мировой онкопрактики вы могли бы отметить как самые яркие? В США, например, сейчас много говорят о так называемой неоадъювантной (дооперационной) терапии.
— Да, мы с американскими коллегами в этом вопросе абсолютно согласны. В этом направлении, кстати, нет ничего нового, и мы тоже им занимаемся. Термин "неоадъювантная терапия" обозначает всегда терапию перед каким-то видом лечения: перед лучевым, хирургическим и так далее. У нас, например, сейчас идет очень интересная неоадъювантная терапия, которая касается рака желудка: когда третью-четвертую стадию нам удается перевести из неоперабельного состояния в операбельное.
Также мы занимаемся радиоэмболизацией и химиоэмболизацией при раке печени, где нам с помощью вот такого неоадъювантного подхода удается достигнуть пятилетней выживаемости пациентов при метастатическом поражении печени. Речь идет о пятилетней выживаемости в 37,8 процентов случаев, — это огромные цифры.
Сейчас наши врачи практикуют также комбинированную лучевую и химиотерапию, тоже в неоадъювантном режиме; это необходимо для того, чтобы довести, подготовить пациента к хирургическому лечению. В настоящее время у нас идут интересные работы и по протоколу лечения рака предстательной железы: так называемые сальважные, то есть «спасительные» операции, когда мы беремся за практически безнадежных пациентов с опухолью предстательной железы и метастазами в региональные лимфоузлы. Мы делаем расширенную простатэктомию с лимфодиссекцией, то есть удаляем и опухоль, и метастазы, после неоадъювантного режима.
Андрей Каприн возглавляет кластер из трех медицинских учреждений — МНИОИ им. П. А. Герцена, МРНЦ им. А. Ф. Цыба и НИИ урологии им. Н. А. Лопаткина. Под его руководством разработаны новые методы комплексного и комбинированного лечения онкологических заболеваний широкого профиля, внедрена в практику брахитерапия различных локализаций, в том числе с помощью разработанного отечественного источника йода-125. Построен первый российский медицинский центр протонной терапии и многое другое.
— Какие новые технологии были внедрены за последнее время в практику НМИЦ радиологии?
— Сейчас активно используем и совершенствуем метод PIPAC-терапии. Это внутрибрюшная аэрозольная химиотерапия, на которую мы берем больных, ранее считавшимися отказными; это пациенты с внутрибрюшной диссеминацией при раке яичника, раке урахуса, раке кишки, диссеминацией по брюшине. Мы уже видим хорошую выживаемость после 12 циклов такой PIPAC-терапии.
Кроме того, у нас сейчас проводятся очень интересные молекулярно-генетические исследования, позволяющие вывести пациентов на лечение по индивидуальной программе. То есть мы делаем конкретно этому пациенту молекулярную диагностику, и, если видим, что никакие из стандартных курсов помогают, разрабатываем для таких больных индивидуальные схемы лечения.
— Говорят же, что медицина будущего — это персонализированная медицина
— Да, именно к этому мы сейчас и идем. В своей практике мы активно используем подбор индивидуальных мишеней для лучевой терапии тоже. Есть различные радиопротекторы, позволяющие их подобрать. Мы ведем разработку пяти новых радионуклидных препаратов. Кстати, хотелось бы поблагодарить за это наше Министерство здравоохранения: в этом году мы впервые за полвека (!) получили приличные деньги для разработки собственных радиофармпрепаратов. Уверен, что их использование станет нашим приоритетным направлением.
— И также в этом году НМИЦ радиологии получил статус референсного центра?
— Все верно. Мы стали референсным центром по лучевой диагностике, молекулярной генетике и патоморфологии с применением дистанционных методов исследований. Эти направления очень важны для нас в научном плане. Кроме того, новый статус очень дисциплинирует коллектив, а также позволят нам работать в рамках телемедицины и оказывать помощь нашим многоуважаемым коллегам из регионов. А еще в этом году мы стали базовой организацией государств-участников стран СНГ в области онкологии.
— Много ли сложных случаев среди онкологических пациентов, с которыми вы работаете? Понятно, что рак сам по себе — уже сложный случай, но с чем обычно связаны наибольшие затруднения в постановке диагноза, в лечении и т.д.?
— Таких случаев колоссальное количество. В целом, онкология связана не только со стандартными случаями. Есть даже целое общество, в котором, кстати, мы являемся одним из экспертных центров. Это Европейская ассоциация редких опухолей. Мы – члены этой Ассоциации, и она достаточно большая. Александр Александрович Феденко и Мамед Джавадович Алиев заслуженно считаются лидерами в этом отношении. Эта организация, естественно, была создана не просто так, а потому что сложных случаев действительно очень много.
К сожалению, существуют очень быстро протекающие заболевания, с высокой степенью злокачественности. Дико растущие опухоли, в которых мы видим колоссальный рост клетки практически без деления. То есть происходит буквально репликация клетки, и этот процесс крайне сложно остановить. Такие заболевания в целом составляют 20% всех злокачественных новообразований. Это целое отдельное направление, целый "космос" в онкологии.
— Нередко часто врачи расходятся во мнениях касательно доброкачественных опухолей, которые так часто возникают у женщин. Андрей Дмитриевич, проясните ситуацию. Киста, миома, фиброаденома, полипы могут перерасти в рак или все-таки нет?
— За всеми из перечисленных новообразований нужно наблюдать. Если мы говорим о фиброаденоме, то важно понять, о каком органе речь. Если это фиброаденома молочной железы, то она однозначно требует наблюдения у врача. Фиброаденома матки — тем более, это вообще одна из самых распространенных локализаций рака у женщин. Яичник тоже требует особого наблюдения, ведь это самая сложная локализация в онкогинекологии. Именно поэтому для женщин, как и для мужчин, выработаны определенные сроки и режим диспансеризации: тот самый онкоскрининг, о котором я так часто говорю в своих выступлениях.
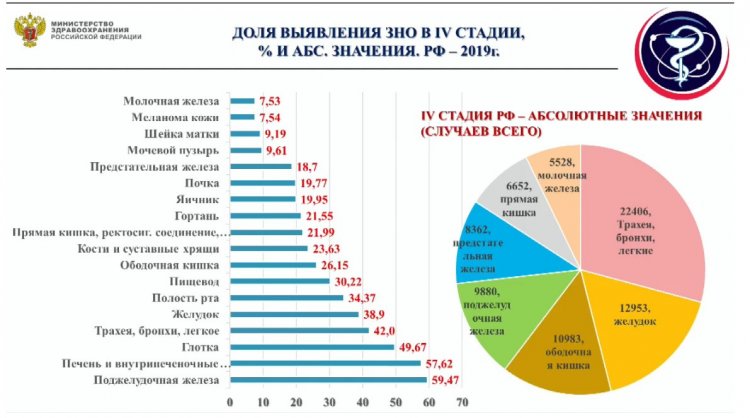
Молочная железа — одна из самых распространенных локализаций рака у женщин, важно вовремя его диагностировать, не допустить перехода на более поздние стадии.
В гинекологии самая распространенная локализация — это тело матки, самая сложная — яичники, самая коварная — шейка матки: вроде и видимая локализация, но можно лечить, например, эрозию, но пропустить рак шейки матки, даже в молодом возрасте.
Из презентации А.Д. Каприна.
— То есть утверждение, что киста, например, в принципе не может перерасти в рак, ошибочно?
— За каждой кистой нужно следить. Бывает, например, киста с пристеночным тканевым компонентом. Это уже опасная киста. Другое дело, если это простая жидкостная киста. Но исследования всех этих кист не просто диагност должен делать, а, скорее, тандем врачей. Диагносты у нас ведь очень разумные и порядочные люди, особенно в онкологии. Они пишут, что "лучевой диагноз не является окончательным, нужен консилиум".
Даже онкологи создают консилиум с лучевыми диагностами, с химиотерапевтами, с другими онкологами. Почему? Потому что каждый случай, каждый пациент может быть не очень простым для восприятия. Сколько мы видели наблюдений за, казалось бы, просто кистой почки, но впоследствии уже с пристеночным ростом злокачественной опухоли этой кисте. Такие моменты прозевать нельзя. А что такое полип, например в мочевом пузыре? Он практически никогда не бывает доброкачественным. Или полип в мочевых путях. Это, как правило, к сожалению, уже работа онколога. Поэтому за такими случаями надо следить обязательно.
— В ваших выступлениях всегда чувствуется основательное знание истории, вы часто говорите о своих предшественниках, об отцах-основателях онкослужбы в нашей стране, приводите интересные факты из их биографии. У вас есть какой-то обязательный минимум художественных и исторических книг для прочтения в год или в месяц? Сколько вообще, на ваш взгляд, нужно читать?
— На самом деле я себя ужасно ругаю за то, что мало читаю, что не прочитываю столько книг, сколько хотелось бы, хотя от чтения получаю колоссальное удовольствие. К сожалению, современная ситуация в стране и профессиональные обязанности требуют, в основном, читать специальную литературу, а я мечтаю и о других книгах. У меня всегда есть несколько начатых, каждую из них я читаю, когда для нее есть время и настроение. Иногда могу зачитаться каким-то художественным произведением и чувствую в ужасе, что я сегодня ничего не посвятил своей профессиональной литературе и начинаю бежать к ней. Не могу вам сказать, кому сколько нужно читать. Это все, конечно, индивидуальная потребность. Заставить себя невозможно: либо хочется, либо нет. Другого не дано. Конечно, тот факт, что любому человеку нужно читать, сомнений ни у кого не вызывает. Лично у меня никакого фиксированного количества книг не по специальности, обязательных к прочтению, нет. Читаю, когда есть время.
— Андрей Дмитриевич, вы могли бы в заключение поздравить коллег с праздником и рассказать нам о своих новогодних ожиданиях?
— С удовольствием! Дорогие мои друзья, многоуважаемые коллеги и коллеги по всем направлениям нашей междисциплинарной онкологии, и дорогие наши работники СМИ, а также те специалисты, без которых наша жизнь вообще была бы невозможной: учителя, педагоги, члены правительства, медсестры, работники транспорта! Словом все, с кем мы живем и работаем бок о бок. Мы ничего друг без друга не представляем. В нашем единении — наша сила. Это показал 2020 год.
Не знаю, почему так произошло в нашей жизни, что мы подверглись подобному испытанию, как COVID-19, и продолжаем подвергаться. Я хотел бы, чтоб оно быстрее закончилось, но осталась та взаимная поддержка, то доброе отношение друг к другу, понимание друг друга, которые нам навязала эта пандемия, заставившая нас вспомнить и проявить все добрые человеческие отношения. Я желаю, чтобы эти добрые отношения никогда не уходили, чтоб они стали еще крепче и существовали и в благоприятное время! Чтобы наша великая страна жила в достатке, с прекрасной нашей верой, с пониманием друг друга, с глубиной понимания. Чтобы мы с вами помнили и детей, и наших стариков, чтоб они были здоровые, наши близкие и родные. И чтобы мы быстрее, пройдя эти испытания, жили в счастливом будущем. Всего вам наилучшего, с наступающим Новым годом!